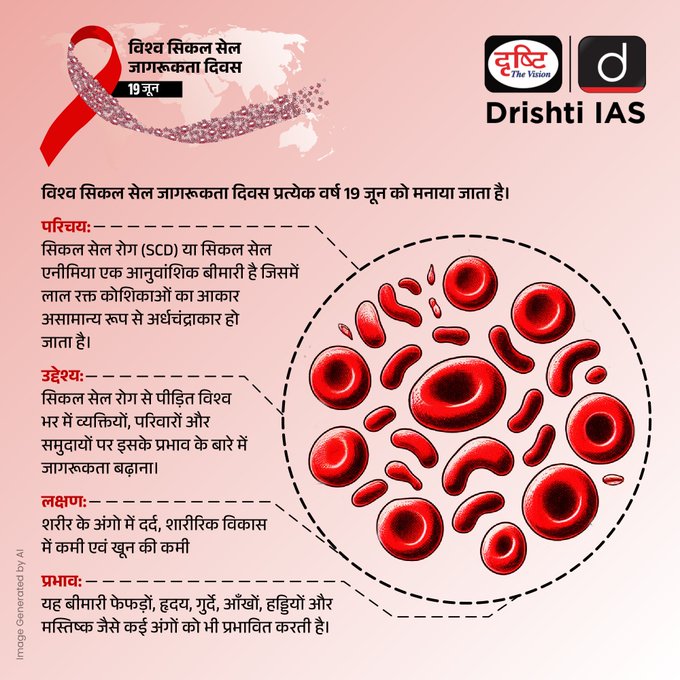
Cet essai clinique de thérapie génique a été mené à l’aide d’une nouvelle technologie de vecteur viral
Cet essai clinique de thérapie génique a été mené à l’aide d’une nouvelle technologie de vecteur viral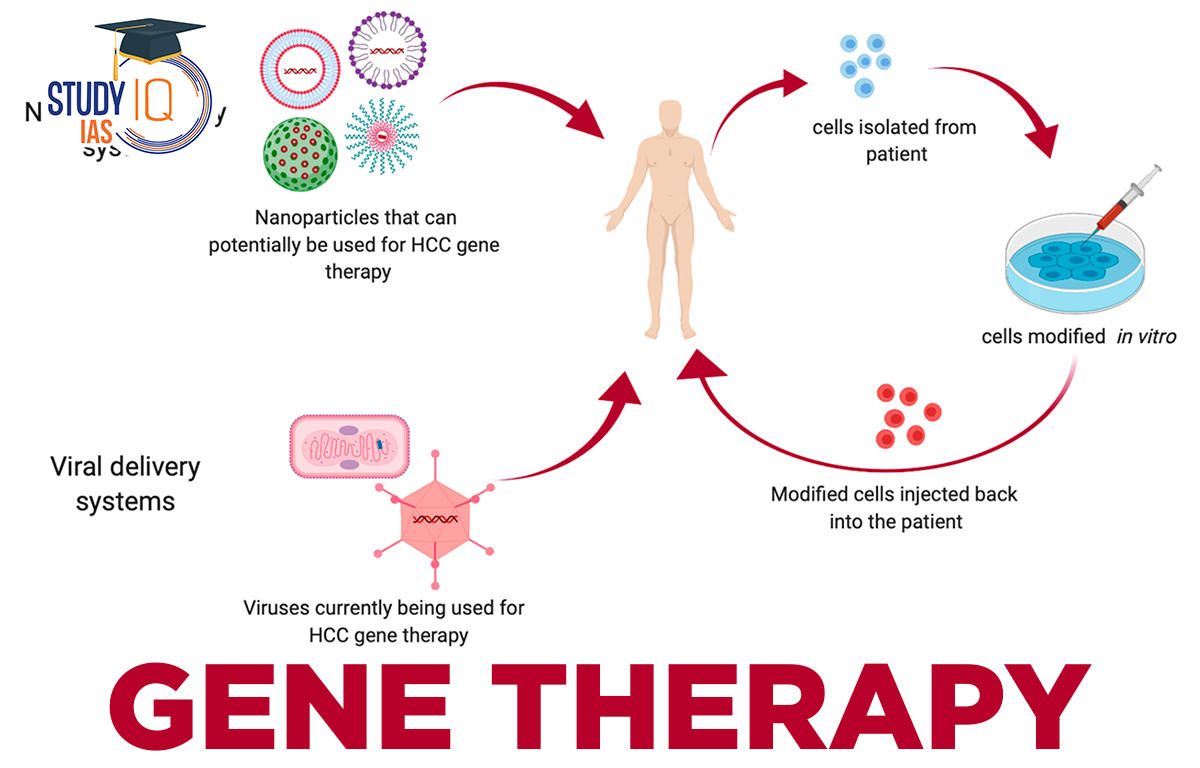 Trente-six ans après la toute première tentative de thérapie génique, seize ans après le premier essai officiellement autorisé, et six ans après le premier indéniable succès thérapeutique, le bilan des multiples efforts investis dans cette approche médicale est bien modeste. Le chiffre d’affaires du secteur, que les pronostics de 1994 évaluaient à plus de vingt milliards de dollars pour 2006, est en réalité quasiment nul : aucun produit de thérapie génique n’est actuellement utilisé, à l’exception de la Gendicine, destinée au traitement des cancers ORL par l’apport du gène p53 et autorisée uniquement en Chine. Que d’espoirs et d’annonces pourtant…
Trente-six ans après la toute première tentative de thérapie génique, seize ans après le premier essai officiellement autorisé, et six ans après le premier indéniable succès thérapeutique, le bilan des multiples efforts investis dans cette approche médicale est bien modeste. Le chiffre d’affaires du secteur, que les pronostics de 1994 évaluaient à plus de vingt milliards de dollars pour 2006, est en réalité quasiment nul : aucun produit de thérapie génique n’est actuellement utilisé, à l’exception de la Gendicine, destinée au traitement des cancers ORL par l’apport du gène p53 et autorisée uniquement en Chine. Que d’espoirs et d’annonces pourtant… 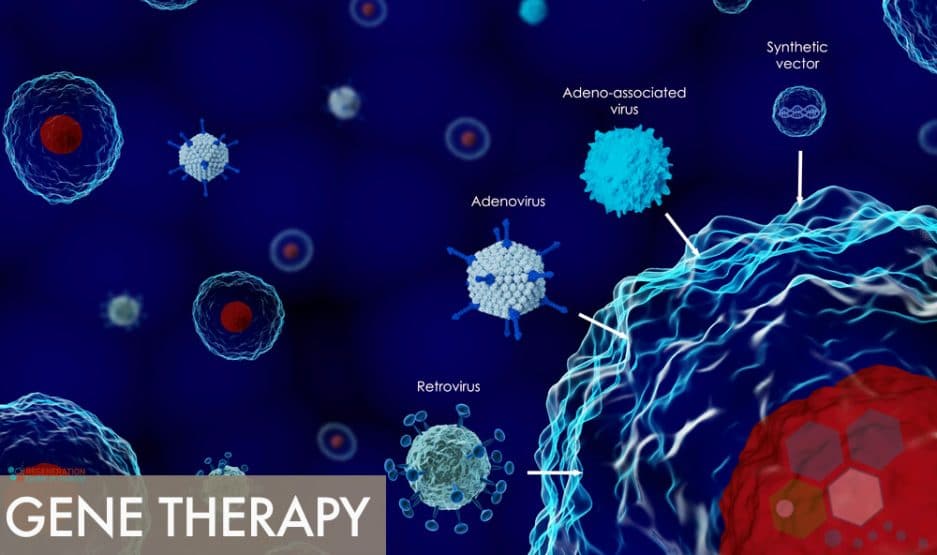 Dès 1985, La Recherche titrait «Traitement des maladies génétiques : le compte à rebours» et prévoyait une montée en puissance rapide des thérapies géniques. Quelques années plus tard, en 1990, la revue Science saluait les premières autorisations dans un article intitulé «Thérapie génique : le but en vue». Pourtant les résultats sur l’animal étaient assez minces ou – s’agissant de transgenèse – non transposables chez l’homme, et les expériences initiales mettaient plus en évidence les difficultés techniques que les possibilités à court terme.
Dès 1985, La Recherche titrait «Traitement des maladies génétiques : le compte à rebours» et prévoyait une montée en puissance rapide des thérapies géniques. Quelques années plus tard, en 1990, la revue Science saluait les premières autorisations dans un article intitulé «Thérapie génique : le but en vue». Pourtant les résultats sur l’animal étaient assez minces ou – s’agissant de transgenèse – non transposables chez l’homme, et les expériences initiales mettaient plus en évidence les difficultés techniques que les possibilités à court terme.  Mais cette thérapie innovante allait dans le sens de l’histoire, et promettait de répondre à des besoins fortement ressentis. Les progrès du diagnostic par analyse de l’ADN (notamment en situation prénatale) n’avaient pas été accompagnés d’avancées médicales équivalentes, et ce décalage croissant soulignait cruellement la nécessité d’approches plus rapides et plus efficaces. L’idée de soigner par l’introduction d’un gène s’accordait aussi avec une vision ultra-réductionniste de la biologie, très en vogue lors du début des Programmes Génome, qui attribuait à l’ADN un rôle central et presque exclusif dans le fonctionnement des organismes : sa lecture allait nous dévoiler les secrets de la vie. Bref, tout était en place pour que l’idée de guérir par les gènes paraisse séduisante et, en somme, naturelle.
Mais cette thérapie innovante allait dans le sens de l’histoire, et promettait de répondre à des besoins fortement ressentis. Les progrès du diagnostic par analyse de l’ADN (notamment en situation prénatale) n’avaient pas été accompagnés d’avancées médicales équivalentes, et ce décalage croissant soulignait cruellement la nécessité d’approches plus rapides et plus efficaces. L’idée de soigner par l’introduction d’un gène s’accordait aussi avec une vision ultra-réductionniste de la biologie, très en vogue lors du début des Programmes Génome, qui attribuait à l’ADN un rôle central et presque exclusif dans le fonctionnement des organismes : sa lecture allait nous dévoiler les secrets de la vie. Bref, tout était en place pour que l’idée de guérir par les gènes paraisse séduisante et, en somme, naturelle. 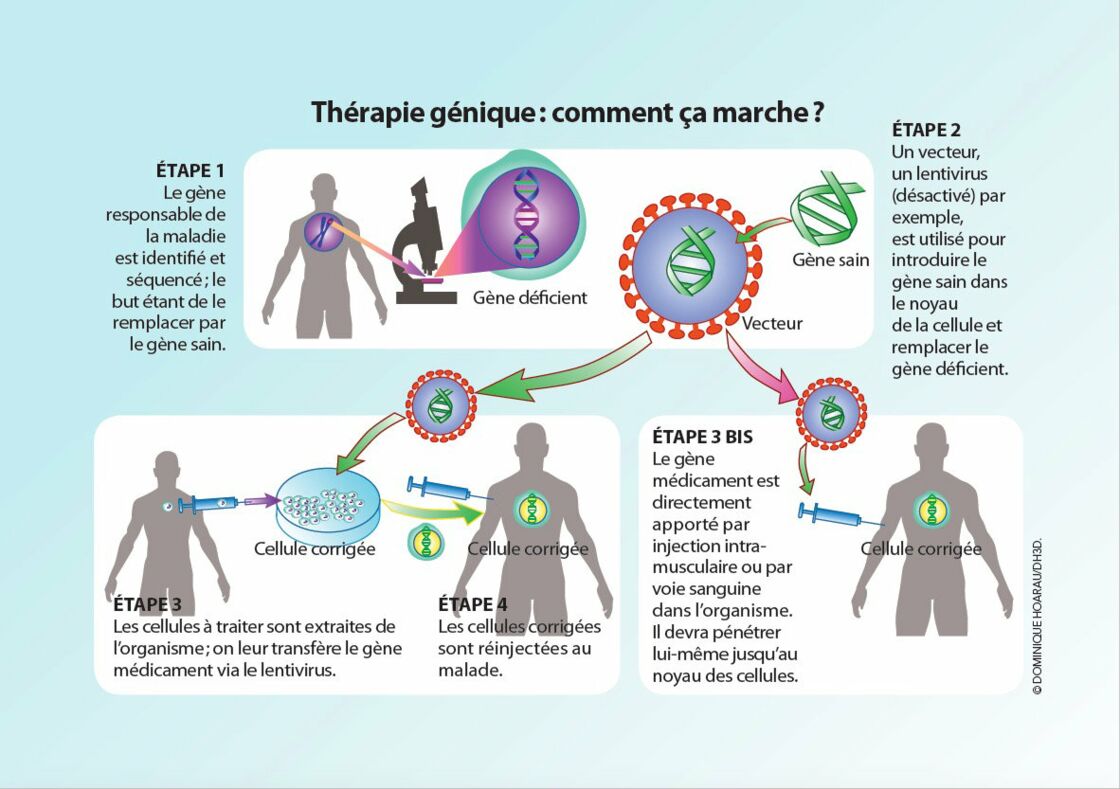 D’autant que cela promettait de contourner les longues étapes de mise au point des traitements classiques, qui impliquent généralement une compréhension détaillée de l’affection puis la découverte d’agonistes ou d’antagonistes agissant sur les éléments-clés des régulations affectées par la maladie… Une expression très employée alors, «L’ADN médicament», exprime bien cet espoir, induisant l’idée qu’une fois le gène introduit, les mécanismes cellulaires allaient «faire leur affaire» de son expression, de sa régulation, et produire à bon escient la protéine thérapeutique. La thérapie génique, enfin, servait de réponse, et éventuellement d’alibi, aux scientifiques et aux institutions que le public commençait à questionner sur les retombées réelles de recherches aussi coûteuses qu’apparemment ésotériques. Les Programmes Génome mobilisaient des sommes colossales. Pour la première fois en biologie, on parlait de milliards de dollars, et les applications thérapeutiques étaient souvent mises en avant pour justifier ces dépenses.
D’autant que cela promettait de contourner les longues étapes de mise au point des traitements classiques, qui impliquent généralement une compréhension détaillée de l’affection puis la découverte d’agonistes ou d’antagonistes agissant sur les éléments-clés des régulations affectées par la maladie… Une expression très employée alors, «L’ADN médicament», exprime bien cet espoir, induisant l’idée qu’une fois le gène introduit, les mécanismes cellulaires allaient «faire leur affaire» de son expression, de sa régulation, et produire à bon escient la protéine thérapeutique. La thérapie génique, enfin, servait de réponse, et éventuellement d’alibi, aux scientifiques et aux institutions que le public commençait à questionner sur les retombées réelles de recherches aussi coûteuses qu’apparemment ésotériques. Les Programmes Génome mobilisaient des sommes colossales. Pour la première fois en biologie, on parlait de milliards de dollars, et les applications thérapeutiques étaient souvent mises en avant pour justifier ces dépenses. 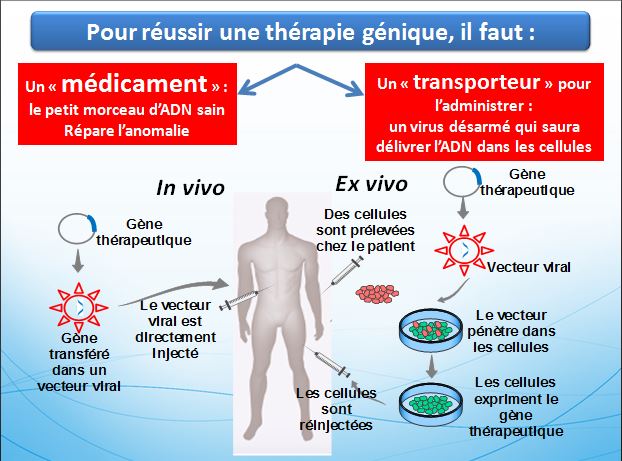 La brochure de présentation du programme américain, en 1995, s’intitulait «Des cartes à la médecine», laissant entendre une liaison directe entre le balisage du génome et les avancées médicales. En France, le slogan du Téléthon 1993, « Des gènes pour guérir », allait dans le même sens, et la communication de l’Association française contre les myopathies (AFM) a durablement mis l’accent sur le soutien aux travaux de thérapie génique, qui ne représentait pourtant qu’un quart environ de ses dépenses. C’est que cette voie apparaissait comme la réponse rêvée à des attentes largement partagées… Ce n’est pas ici le lieu de détailler les multiples problèmes techniques auxquels s’est heurtée la mise au point de thérapies géniques réellement utilisables. Ils sont nombreux, depuis le développement de vecteurs efficaces et sûrs (ces deux qualités étant le plus souvent contradictoires) jusqu’à la maîtrise de la réaction immunitaire du patient envers la nouvelle protéine apportée …
La brochure de présentation du programme américain, en 1995, s’intitulait «Des cartes à la médecine», laissant entendre une liaison directe entre le balisage du génome et les avancées médicales. En France, le slogan du Téléthon 1993, « Des gènes pour guérir », allait dans le même sens, et la communication de l’Association française contre les myopathies (AFM) a durablement mis l’accent sur le soutien aux travaux de thérapie génique, qui ne représentait pourtant qu’un quart environ de ses dépenses. C’est que cette voie apparaissait comme la réponse rêvée à des attentes largement partagées… Ce n’est pas ici le lieu de détailler les multiples problèmes techniques auxquels s’est heurtée la mise au point de thérapies géniques réellement utilisables. Ils sont nombreux, depuis le développement de vecteurs efficaces et sûrs (ces deux qualités étant le plus souvent contradictoires) jusqu’à la maîtrise de la réaction immunitaire du patient envers la nouvelle protéine apportée …
 L’histoire et l’évolution de la thérapie génique
L’histoire et l’évolution de la thérapie génique
Bien que seul un petit nombre de thérapies géniques soient actuellement approuvées, la thérapie génique n’est pas une nouvelle approche pour traiter les maladies. Découvrez comment des années de recherche scientifique et clinique dans ce domaine nous ont conduits au monde de la thérapie génique d’aujourd’hui.Façonner la thérapie génique
Les chercheurs spécialisés dans les maladies génétiques se posent la même question depuis des décennies : et si on pouvait traiter une maladie héréditaire ou un cancer au niveau génétique ?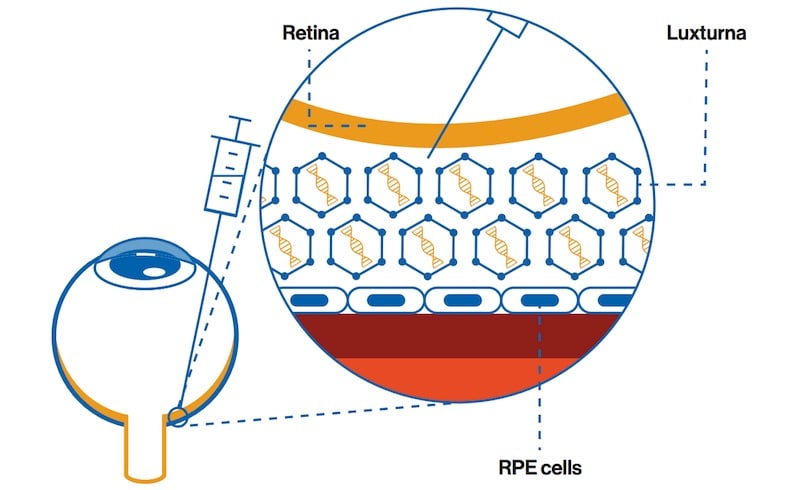 La plupart des chercheurs croyaient que la thérapie génique était possible dès le début. Mais il a fallu des décennies de travail acharné, une meilleure compréhension de la génétique et la découverte de techniques susceptibles de traiter les maladies héréditaires et les cancers au niveau génétique.
La plupart des chercheurs croyaient que la thérapie génique était possible dès le début. Mais il a fallu des décennies de travail acharné, une meilleure compréhension de la génétique et la découverte de techniques susceptibles de traiter les maladies héréditaires et les cancers au niveau génétique.
Ces dernières années, la thérapie génique a fait de grands progrès. Maintenant, il continue de progresser de la recherche au pipeline de la Food and Drug Administration (FDA) des États-Unis examen et approbations potentielles, dans le but ultime de servir les populations de patients susceptibles d’en bénéficier. Histoire de la thérapie génique
Histoire de la thérapie génique
La thérapie génique a évolué au fil des ans. Voici quelques-unes des étapes les plus importantes qui nous ont amenés là où nous en sommes aujourd’hui avec la thérapie génique : 1953 La structure de l’ADN était caractérisée par une double hélice
1953 La structure de l’ADN était caractérisée par une double hélice
James Watson, Francis Crick, Maurice Wilkins et Rosalind Franklin
1961-1966 Le code génétique a été découvert en déchiffrant les trois bases de l’ADN dans 1 des 20 acides aminés. Les 19 acides aminés restants ont été déchiffrés peu après, ouvrant la voie à de nouvelles technologies 1973 Les chercheurs ont découvert une technique de génie génétique qui permet au matériel génétique d’un organisme d’être artificiellement introduit, reproduit et exprimé dans 5 autres
1973 Les chercheurs ont découvert une technique de génie génétique qui permet au matériel génétique d’un organisme d’être artificiellement introduit, reproduit et exprimé dans 5 autres L’ADN a été épissé dans un vecteur plasmidique (une structure d’ADN qui peut se répliquer sans chromosome), qui a ensuite inséré du matériel génétique dans une bactérie E. coli. Lorsque la bactérie s’est reproduite, elle a répliqué l’ADN étranger et conservé le matériel génétique de l’organisme d’origine.
L’ADN a été épissé dans un vecteur plasmidique (une structure d’ADN qui peut se répliquer sans chromosome), qui a ensuite inséré du matériel génétique dans une bactérie E. coli. Lorsque la bactérie s’est reproduite, elle a répliqué l’ADN étranger et conservé le matériel génétique de l’organisme d’origine.
1980 L’une des premières fois que la thérapie génique a été testée sur des personnes a été effectuée sans l’autorisation de l’université qui a financé les National Institutes of Health (NIH). Le chercheur a perdu plusieurs subventions et le NIH a averti les autres que l’expérimentation humaine ne serait pas tolérée Martin Cline a tenté une thérapie génique à l’étranger sans autorisation chez 2 patients atteints de bêta-thalassémie, une maladie sanguine héréditaire rare, en transférant le gène de la bêta-globine dans leurs cellules. Cela n’a pas fonctionné car les cellules ne se sont pas répliquées
Martin Cline a tenté une thérapie génique à l’étranger sans autorisation chez 2 patients atteints de bêta-thalassémie, une maladie sanguine héréditaire rare, en transférant le gène de la bêta-globine dans leurs cellules. Cela n’a pas fonctionné car les cellules ne se sont pas répliquées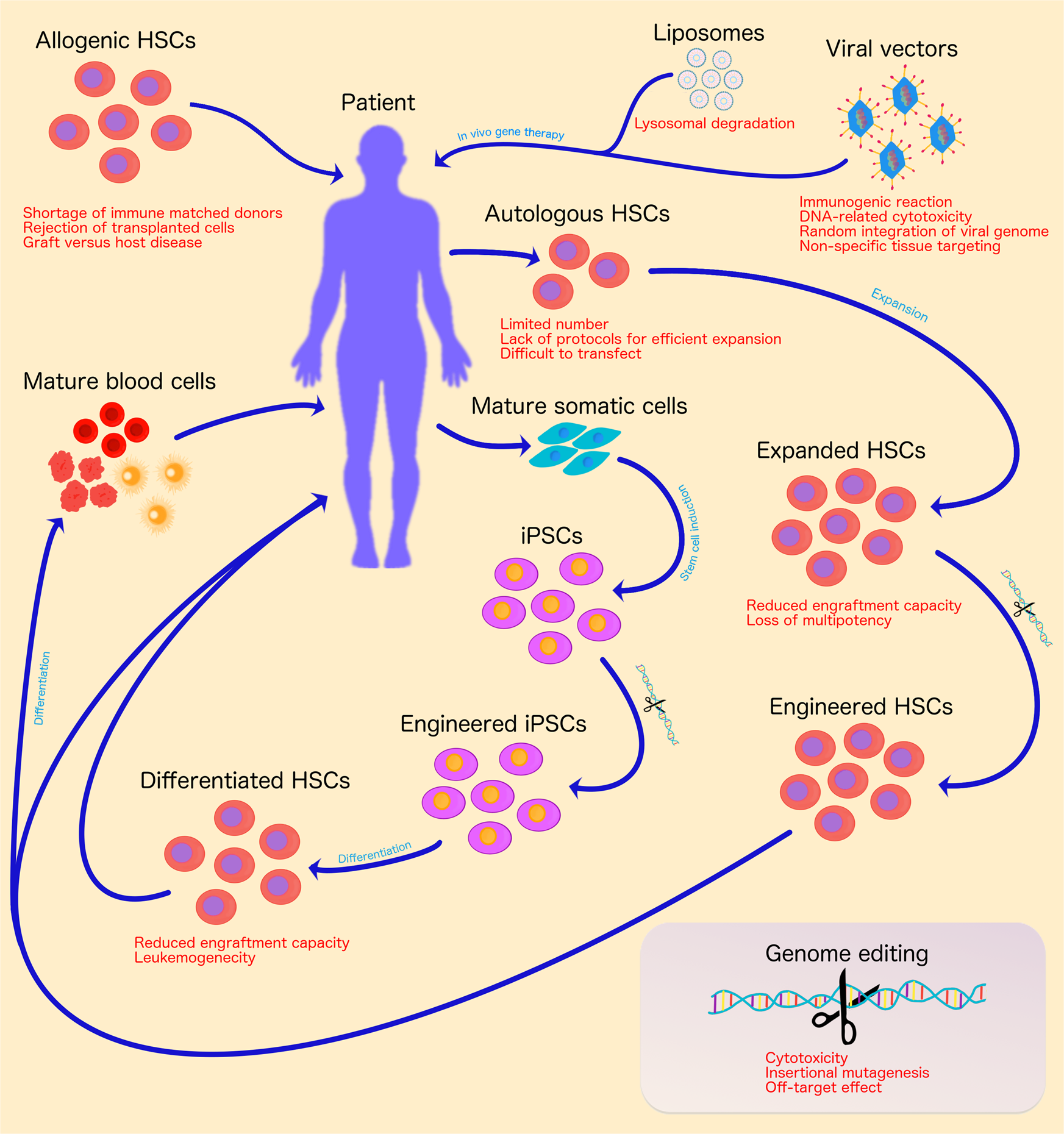 1990 Le premier essai clinique de thérapie génique a été mené à l’aide d’une nouvelle technologie de vecteur viral
1990 Le premier essai clinique de thérapie génique a été mené à l’aide d’une nouvelle technologie de vecteur viral
2 patients atteints d’immunodéficience combinée sévère (SCID) ont reçu un traitement utilisant une nouvelle technologie de vecteur de rétrovirus gamma. Les résultats étaient mitigés, avec 1 réponse modeste et 1 réponse limitée 1996 La première technologie de nucléase modifiée (nucléase à doigts de zinc) a été étudiée, jetant les bases de l’exploration de l’utilisation des nucléases à doigts de zinc pour l’édition de gènes en tant que potentiel de thérapie génique
1996 La première technologie de nucléase modifiée (nucléase à doigts de zinc) a été étudiée, jetant les bases de l’exploration de l’utilisation des nucléases à doigts de zinc pour l’édition de gènes en tant que potentiel de thérapie génique
1996 La première génération de vecteurs lentiviraux (LVV) a été créée à l’aide de 3 plasmides différents (une structure d’ADN qui peut se répliquer sans chromosome) contenant une grande partie désactivée du génome du VIH, ce qui rend peu probable la réplication du VIH dans les cellules humaines
Les LVV de deuxième et troisième génération ont suivi quelques années plus tard, contenant une réduction supplémentaire du génome original du VIH (moins des deux tiers) 1999 La FDA et le NIH ont créé de nouveaux programmes – le plan de surveillance des essais cliniques de thérapie génique et les symposiums sur la sécurité du transfert de gènes – dans le but d’assurer la sécurité et la transparence des essais cliniques de thérapie génique. C’était après le décès d’un patient de 18 ans lors d’un essai clinique utilisant un vecteur adénoviral. Une protection supplémentaire des patients a entraîné des retards dans la recherche à l’époque, mais a conduit à mettre davantage l’accent sur la sécurité et le partage des données depuis dans les efforts de recherche sur la thérapie génique.
1999 La FDA et le NIH ont créé de nouveaux programmes – le plan de surveillance des essais cliniques de thérapie génique et les symposiums sur la sécurité du transfert de gènes – dans le but d’assurer la sécurité et la transparence des essais cliniques de thérapie génique. C’était après le décès d’un patient de 18 ans lors d’un essai clinique utilisant un vecteur adénoviral. Une protection supplémentaire des patients a entraîné des retards dans la recherche à l’époque, mais a conduit à mettre davantage l’accent sur la sécurité et le partage des données depuis dans les efforts de recherche sur la thérapie génique.
Jesse Gelsinger, un garçon de 18 ans atteint d’une forme relativement bénigne de déficit en ornithine transcarbamylase (OTC), est décédé alors qu’il participait à un essai de thérapie génique adénovirale en raison d’une réaction immunitaire sévère au vecteur. Les enquêteurs ont découvert plus tard que plusieurs autres patients avaient subi des effets secondaires graves après avoir été injectés, mais Jesse n’en a jamais été informé. Cela a amené la FDA et le NIH à améliorer la protection des patients grâce à 2 nouveaux programmes, le plan de surveillance des essais cliniques de thérapie génique et les symposiums sur la sécurité du transfert de gènes.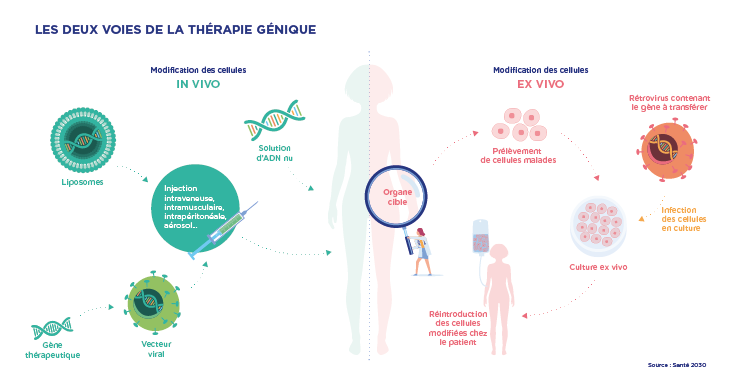 2000 Un essai clinique de thérapie génique utilisant un rétrovirus gamma a soulevé des inquiétudes quant à la sécurité de l’insertion de gènes
2000 Un essai clinique de thérapie génique utilisant un rétrovirus gamma a soulevé des inquiétudes quant à la sécurité de l’insertion de gènes
Dix patients atteints d’immunodéficience combinée sévère liée à l’X (SCID) ont été traités par thérapie génique. Alors que 9 patients sur 10 ont été traités, 4 des 9 patients ont développé une leucémie. Cette étude a démontré le besoin de vecteurs viraux améliorés en thérapie génique
2002 La FDA a approuvé le premier essai clinique (chez l’homme) utilisant un LVV pour tester l’innocuité et la tolérabilité d’une seule perfusion chez des patients infectés par le VIH. L’essai de phase 1 s’est achevé avec succès, ouvrant la porte à d’autres recherches sur le LVV, y compris un essai de phase 2 2003 La National Medical Products Administration, anciennement China Food and Drug Administration, a approuvé la première thérapie génique disponible dans le commerce au monde pour traiter le carcinome épidermoïde, une forme de cancer de la peau
2003 La National Medical Products Administration, anciennement China Food and Drug Administration, a approuvé la première thérapie génique disponible dans le commerce au monde pour traiter le carcinome épidermoïde, une forme de cancer de la peau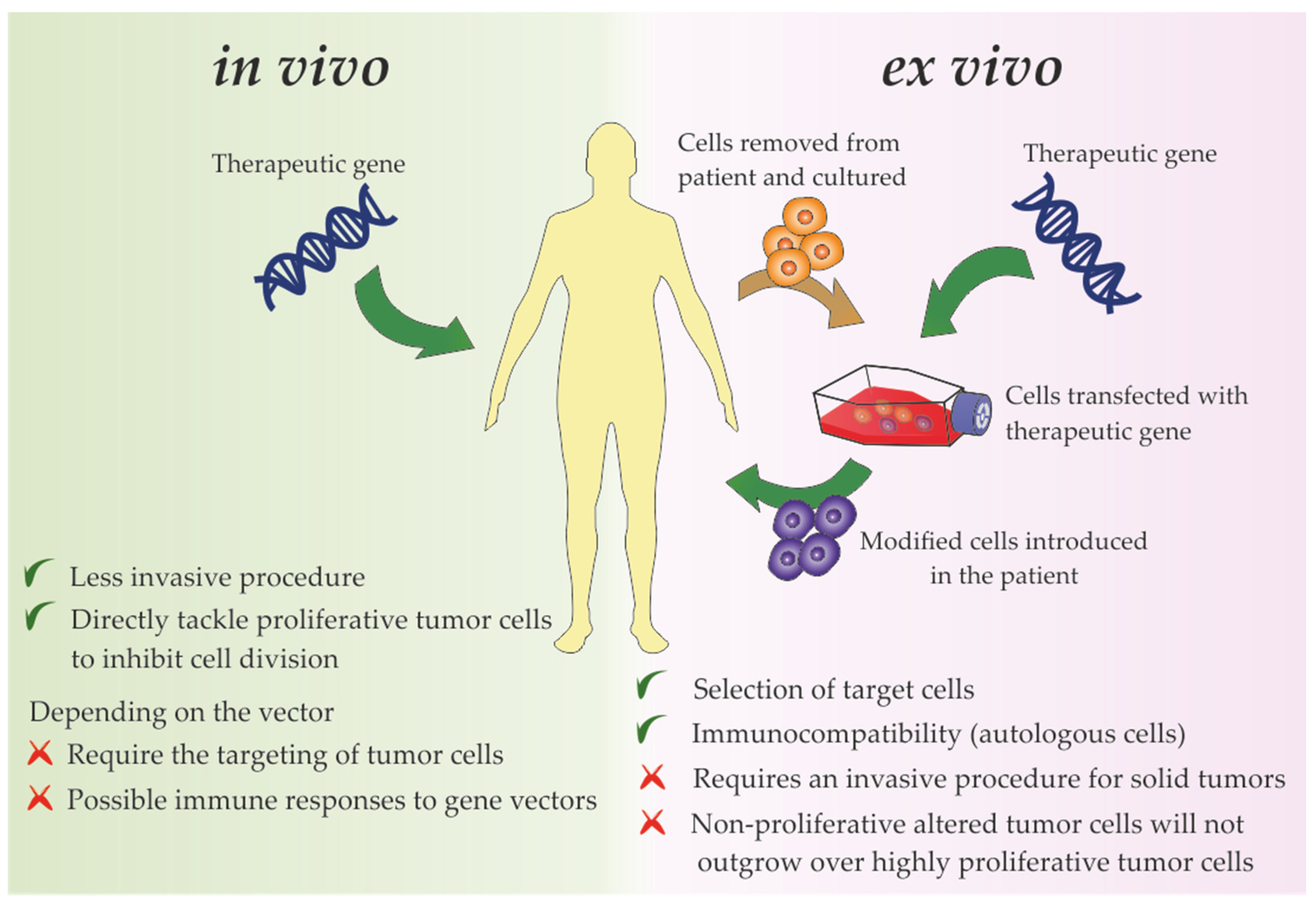 2009 Dans un essai clinique, une maladie oculaire génétique a été traitée à l’aide d’un vecteur de virus adéno-associé (AAV). Huit ans plus tard, cet essai pivot a conduit à l’approbation par la FDA de la première thérapie génique aux États-Unis
2009 Dans un essai clinique, une maladie oculaire génétique a été traitée à l’aide d’un vecteur de virus adéno-associé (AAV). Huit ans plus tard, cet essai pivot a conduit à l’approbation par la FDA de la première thérapie génique aux États-Unis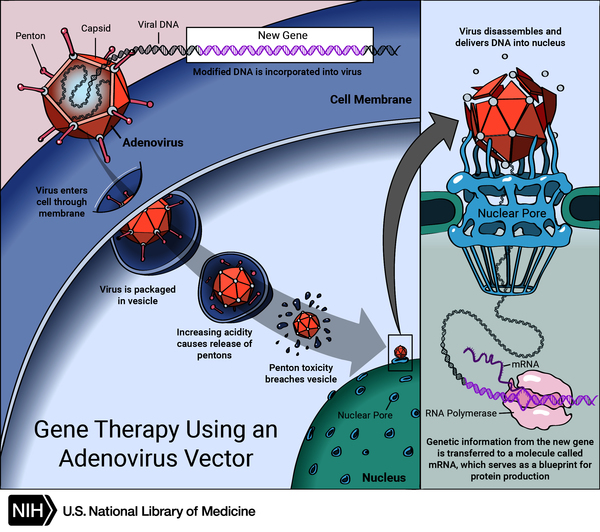 2010 Les premières nucléases effectrices TAL modifiées ont été décrites avec la capacité de provoquer une mutagenèse ciblée
2010 Les premières nucléases effectrices TAL modifiées ont été décrites avec la capacité de provoquer une mutagenèse ciblée 2010 Un LVV auto-inactivant a été utilisé pour la première fois dans des essais cliniques de thérapie par addition de gènes dans les hémoglobinopathies
2010 Un LVV auto-inactivant a été utilisé pour la première fois dans des essais cliniques de thérapie par addition de gènes dans les hémoglobinopathies
2012 L’Agence européenne des médicaments (EMA) a approuvé la première thérapie par addition génique basée sur l’AAV pour le traitement du déficit en lipoprotéine lipase (LPLD)
Cette thérapie génique a ensuite été retirée du marché en 2017 en raison de son utilisation limitée 2012 Les scientifiques ont développé une technique d’édition de gènes appelée CRISPR/Cas9 qui peut modifier des séquences d’ADN spécifiques
2012 Les scientifiques ont développé une technique d’édition de gènes appelée CRISPR/Cas9 qui peut modifier des séquences d’ADN spécifiques
2016 L’EMA a approuvé la première thérapie par addition génique basée sur le rétrovirus gamma pour traiter l’immunodéficience combinée sévère à l’adénosine désaminase (ADA-SCID). Cette thérapie contient des cellules CD34+ transduites avec un vecteur rétroviral, qui code pour la séquence d’ADNc de l’ADA humaine 2017 La FDA a approuvé la première thérapie par addition de gènes in vivo pour traiter les patients atteints d’une forme rare de cécité héréditaire appelée dystrophie rétinienne associée à la mutation biallélique RPE65
2017 La FDA a approuvé la première thérapie par addition de gènes in vivo pour traiter les patients atteints d’une forme rare de cécité héréditaire appelée dystrophie rétinienne associée à la mutation biallélique RPE65
2017 La FDA a approuvé une thérapie CAR T-cell pour le traitement des patients atteints d’un lymphome à grandes cellules B récidivant/réfractaire (LDGCB R/R).
Approuvé par l’EMA en 2019 2018 Le premier essai clinique utilisant CRISPR/Cas9 a été lancé. Cette étude étudie l’utilisation de CRISPR/Cas9 pour la perturbation des gènes dans les bêta-hémoglobinopothies
2018 Le premier essai clinique utilisant CRISPR/Cas9 a été lancé. Cette étude étudie l’utilisation de CRISPR/Cas9 pour la perturbation des gènes dans les bêta-hémoglobinopothies
2019 La FDA a approuvé une thérapie d’addition génique in vivo basée sur l’AAV pour l’amyotrophie spinale
Approbation conditionnelle par l’EMA en 2020 29
2019 L’EMA a approuvé une thérapie par addition génique ex vivo basée sur le LVV pour une maladie génétique appelée bêta-thalassémie dépendante de la transfusion (TDT)
2020 La FDA finalise 6 lignes directrices sur la thérapie génique, y compris un projet de lignes directrices pour la recherche et le développement clinique des thérapies géniques
2021 Un nouveau-né de 4 jours a reçu une thérapie génique in vivo pour l’amyotrophie spinale, faisant d’elle la plus jeune patiente à ce stade à recevoir une thérapie génique
Entrer dans l’histoire avec l’essai de thérapie génique
Alors qu’elle n’avait que deux jours, Ashanti DeSilva a développé une infection. Il s’est avéré que c’était la première des nombreuses infections qui déconcertaient ses parents et ses médecins jusqu’à l’âge de 26 mois, lorsqu’elle a finalement reçu un diagnostic de déficit en adénosine désaminase (ADA), une forme de maladie d’immunodéficience combinée (SCID) sévère.
Comme d’autres enfants atteints de la maladie, DeSilva a commencé à prendre de l’ADA pégylé (PEG-ADA), une thérapie enzymatique apparue dans les années 1980. Le traitement a suffisamment fonctionné pour qu’elle prenne du poids, développe un nombre normal de lymphocytes T périphériques et subisse moins d’infections. Pourtant, son déficit immunitaire persistait.
À l’âge de quatre ans, DeSilva est entré dans l’histoire à 12 h 52 le 14 septembre 1990, en tant que premier patient à subir une application approuvée de thérapie génique. Elle faisait partie d’un essai autorisé par la FDA et le NIH’s Recombinant DNA Advisory Committee (RAC). L’essai ne comprenait qu’une seule autre patiente, Cynthia Cutshall (aujourd’hui Kisik). Cynthia a commencé le traitement le 31 janvier 1991, alors qu’elle avait neuf ans.
Les chercheurs ont prélevé du sang sur les deux filles, incitant les lymphocytes T de leur sang à se répliquer en culture. Des vecteurs rétroviraux infusés avec des gènes ADA fonctionnels ont été transférés dans les cellules T cultivées. Les lymphocytes T corrigés par le gène ont été réinjectés aux filles environ 12 jours après le prélèvement de sang. DeSilva a reçu 11 perfusions sur environ deux ans, contre 12 perfusions sur 18 mois pour Cutshall.
L’essai, qui a eu lieu au centre clinique des NIH, a été dirigé par W. French Anderson, MD, alors du National Heart, Lung, and Blood Institute des NIH ; R. Michael Blaese, MD, alors chef de la section d’immunologie cellulaire du National Cancer Institute (NCI) des NIH ; et Kenneth W. Culver, MD, alors également du NCI, dans le laboratoire du Dr Blaese. Les chercheurs ont utilisé un vecteur rétroviral ADA construit et fourni par A. Dusty Miller, PhD., du Fred Hutchinson Cancer Center à Seattle.
« Nous avons essentiellement montré que vous pouviez le faire, que vous pouviez le faire en toute sécurité et que vous pouviez avoir un impact positif sur les patients », a déclaré à GEN le Dr Blaese, qui était également chef adjoint de la branche métabolisme du NCI. « Ce n’était pas un essai curatif, mais c’était certainement un traitement efficace, et je pense que cela a ouvert la porte à des essais très réussis qui ont guéri des patients d’un certain nombre de maladies. »
Thérapie génique
En 1990, les expériences de thérapie génique par l’insertion de nouveaux gènes dans les cellules du corps ont été approuvées pour la première fois par le comité consultatif sur l’ADN recombinant des National Institutes of Health. Ces premières véritables thérapies géniques pour l’homme concernaient le déficit en adénosine désaminase (une maladie génétique qui détruit le système immunitaire) et une forme de cancer. Le Dr McGarrity, président du comité, a noté que les protocoles sur lesquels ils avaient voté étaient les premières approbations d’une véritable thérapie génique plutôt qu’une simple insertion de gènes. Le Dr Garrity a ajouté qu’il s’agissait d’un événement historique dans la mesure où la thérapie génique peut désormais s’ajouter au répertoire des vaccins, des antibiotiques, des médicaments, de la chirurgie et des radiations pour combattre
https://www.genengnews.com/magazine/269/making-history-with-the-1990-gene-therapy-trial/
https://www.erudit.org/fr/revues/ms/2006-v22-n5-ms1287/013163ar/resume/