 Synthèse d’ammoniac – L’épée à double tranchant
Synthèse d’ammoniac – L’épée à double tranchant  Haber, l’ammoniac et un héritage complexe
Haber, l’ammoniac et un héritage complexe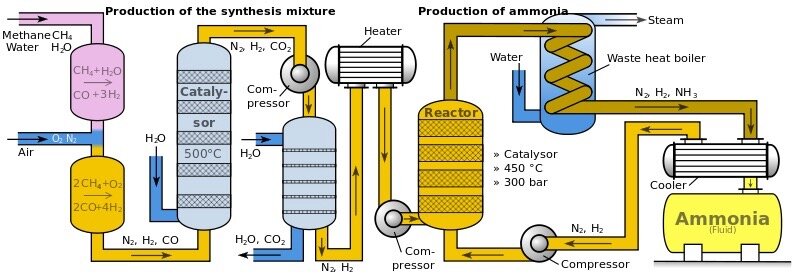 En 1910, un brevet américain pour la production d’ammoniac a été délivré à Fritz Haber (1868-1934) et Robert Le Rossignol (n ° 971 501). Ce processus pourrait produire de l’ammoniac à grande échelle directement à partir de ses gaz composants, l’hydrogène et l’azote, en faisant passer un mélange de ceux-ci sur de l’osmium métallique finement divisé chauffé utilisé comme catalyseur.
En 1910, un brevet américain pour la production d’ammoniac a été délivré à Fritz Haber (1868-1934) et Robert Le Rossignol (n ° 971 501). Ce processus pourrait produire de l’ammoniac à grande échelle directement à partir de ses gaz composants, l’hydrogène et l’azote, en faisant passer un mélange de ceux-ci sur de l’osmium métallique finement divisé chauffé utilisé comme catalyseur. 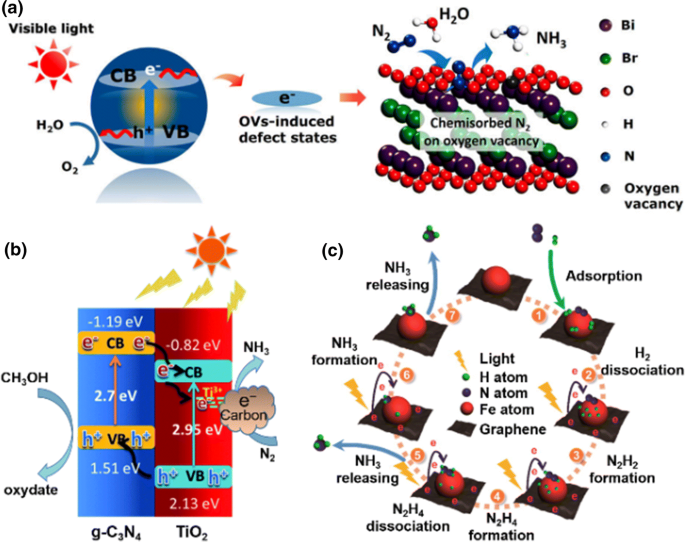 Une pression typique de 175 atmosphères et une température de 550 ºC pourraient facilement donner un rendement de 8 % en volume d’ammoniac. Bien que l’azote constitue 80% de l’air, en tant que gaz, il est assez peu réactif. Malgré sa disponibilité immédiate, l’azote gazeux était auparavant difficile à combiner sous une forme chimique. Une fois que l’azote a été combiné chimiquement sous forme d’ammoniac, de nombreux autres composés azotés peuvent être fabriqués.
Une pression typique de 175 atmosphères et une température de 550 ºC pourraient facilement donner un rendement de 8 % en volume d’ammoniac. Bien que l’azote constitue 80% de l’air, en tant que gaz, il est assez peu réactif. Malgré sa disponibilité immédiate, l’azote gazeux était auparavant difficile à combiner sous une forme chimique. Une fois que l’azote a été combiné chimiquement sous forme d’ammoniac, de nombreux autres composés azotés peuvent être fabriqués.  Antisémitisme croissant
Antisémitisme croissant
En 1901, Haber avait épousé Clara Immerwahr, une brillante chimiste et la première femme à obtenir un doctorat de l’Université de Breslau. Même si elle s’est également convertie du judaïsme au christianisme comme Haber, le couple était toujours sujet à l’antisémitisme (discrimination contre les juifs). Au tournant du siècle, il y avait un murmure croissant, en particulier parmi les scientifiques, que le monde ne serait pas en mesure de faire face à la demande alimentaire croissante de la population croissante de l’humanité. Alors qu’il était bien connu à cette époque que les engrais à base d’azote seraient capables d’améliorer le rendement des cultures et donc de répondre à la demande à venir, la fixation de l’azote de l’air n’était pas encore réalisée. Fixation de l’azote
Fixation de l’azote
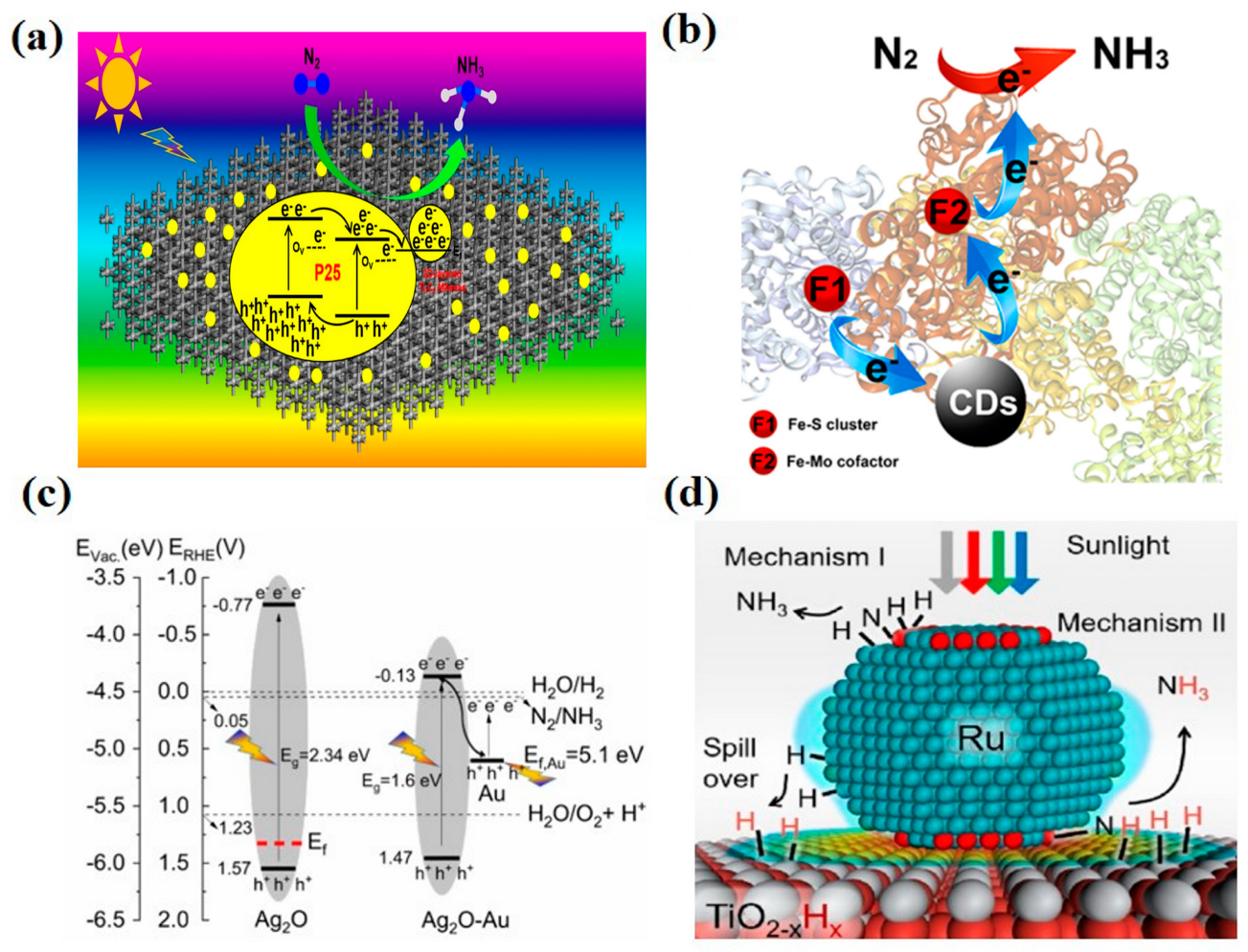 Le 27 septembre 1910, Haber a reçu un brevet américain pour la production d’ammoniac. En collaboration avec le chimiste et ingénieur allemand de la société chimique BASF, Carl Bosch, le processus de création d’ammoniac à partir d’azote atmosphérique a été intensifié. Le procédé Haber-Bosch est né, permettant de créer de grandes quantités d’ammoniac.
Le 27 septembre 1910, Haber a reçu un brevet américain pour la production d’ammoniac. En collaboration avec le chimiste et ingénieur allemand de la société chimique BASF, Carl Bosch, le processus de création d’ammoniac à partir d’azote atmosphérique a été intensifié. Le procédé Haber-Bosch est né, permettant de créer de grandes quantités d’ammoniac.
«Pain sorti de nulle part» L’ammoniac ainsi produit pourrait être utilisé à des fins industrielles, créant d’énormes quantités d’engrais. Les engrais agricoles ont augmenté le rendement des cultures dans une large mesure, mettant fin à la peur des famines et produisant suffisamment de nourriture pour subvenir aux besoins croissants de l’humanité. «Brot aus luft», qui signifie littéralement «pain sorti de nulle part», était le slogan allemand populaire utilisé à l’époque pour désigner ce revirement miraculeux. Haber a toujours voulu prouver son patriotisme et il a donc jeté ses efforts derrière la cause allemande pendant la Première Guerre mondiale. Il a expérimenté le chlore gazeux et a développé une nouvelle arme, le gaz toxique, qui, selon lui, raccourcirait la guerre.
L’ammoniac ainsi produit pourrait être utilisé à des fins industrielles, créant d’énormes quantités d’engrais. Les engrais agricoles ont augmenté le rendement des cultures dans une large mesure, mettant fin à la peur des famines et produisant suffisamment de nourriture pour subvenir aux besoins croissants de l’humanité. «Brot aus luft», qui signifie littéralement «pain sorti de nulle part», était le slogan allemand populaire utilisé à l’époque pour désigner ce revirement miraculeux. Haber a toujours voulu prouver son patriotisme et il a donc jeté ses efforts derrière la cause allemande pendant la Première Guerre mondiale. Il a expérimenté le chlore gazeux et a développé une nouvelle arme, le gaz toxique, qui, selon lui, raccourcirait la guerre.
Haber a supervisé le premier déploiement de ses méthodes à Ypres, en Belgique, en 1915 et il a été promu capitaine dans l’armée allemande. Le soir où il a célébré sa promotion lors d’une fête chez lui à Berlin, Clara, qui condamnait les travaux d’armes de son mari et devenait frustrée par la vie à la maison, s’est suicidée. Le suicide de sa femme n’a pas retardé son déploiement alors qu’il se précipitait vers le front de guerre. Mais beaucoup d’autres ont commencé à exprimer leur opinion sur le rôle de Haber en temps de guerre et sur ce qu’ils considéraient comme la promotion d’une arme barbare. Lorsqu’il reçut le prix Nobel de chimie en 1918 pour la synthèse de l’ammoniac à partir de ses éléments, cela ne convenait naturellement pas à tout le monde.
Fuit l’Allemagne 
Alors que Haber continuait à lutter patriotiquement, il pouvait sentir qu’il était toujours pris dans la toile de l’antisémitisme. Lorsque les nazis gagnaient en puissance, il était encore perçu comme un Juif et sa position devint rapidement intenable. Il a fui l’Allemagne et s’est exilé, mais n’a pas trouvé de travail ni d’endroit où s’installer, mourant finalement d’une crise cardiaque en 1934. Outre le gaz toxique, les recherches de Haber ont également été développées plus tard dans le procédé Zyklon. Cela a été utilisé par les nazis pour tuer des millions de personnes dans leurs camps de concentration, y compris certains des propres parents élargis de Haber. Malgré l’importance de son travail pour produire de l’ammoniac, qui aide toujours l’agriculture dans le monde entier, Haber a laissé un héritage compliqué, en grande partie à cause de ses efforts sur le front de guerre. Le physicien théoricien d’origine allemande Albert Einstein a résumé la vie de son ami et sa relation avec sa patrie de la manière suivante : « La vie de Haber était la tragédie du Juif allemand – la tragédie de l’amour non partagé. »
Synthèse d’ammoniac – L’épée à double tranchant
 Fritz Haber a déposé un brevet allemand en 1908 pour la synthèse de l’ammoniac pour lequel il a remporté un prix Nobel de chimie en 1918. C’était une invention véritablement révolutionnaire ; Haber a découvert comment l’ammoniac, une forme d’azote chimiquement réactive et hautement utilisable, pouvait être synthétisé. Un sol naturellement riche en azote est une terre agricole de choix en raison de sa productivité élevée, mais l’azote s’épuise à chaque récolte, ce qui réduit le rendement des terres agricoles d’année en année. Un moyen de restituer l’azote au sol conduirait à une récolte continue et abondante. Notre atmosphère est composée à 78 % d’azote, mais il existe sous une forme chimiquement et biologiquement inutilisable. Grâce à la découverte de Haber, l’azote bon marché est devenu facilement disponible et facilement utilisable comme engrais. La synthèse d’ammoniac a augmenté de manière exponentielle les récoltes et continuera de le faire pendant des années. Son invention est créditée d’avoir sauvé des millions de vies et en sauvera probablement des milliards d’autres.
Fritz Haber a déposé un brevet allemand en 1908 pour la synthèse de l’ammoniac pour lequel il a remporté un prix Nobel de chimie en 1918. C’était une invention véritablement révolutionnaire ; Haber a découvert comment l’ammoniac, une forme d’azote chimiquement réactive et hautement utilisable, pouvait être synthétisé. Un sol naturellement riche en azote est une terre agricole de choix en raison de sa productivité élevée, mais l’azote s’épuise à chaque récolte, ce qui réduit le rendement des terres agricoles d’année en année. Un moyen de restituer l’azote au sol conduirait à une récolte continue et abondante. Notre atmosphère est composée à 78 % d’azote, mais il existe sous une forme chimiquement et biologiquement inutilisable. Grâce à la découverte de Haber, l’azote bon marché est devenu facilement disponible et facilement utilisable comme engrais. La synthèse d’ammoniac a augmenté de manière exponentielle les récoltes et continuera de le faire pendant des années. Son invention est créditée d’avoir sauvé des millions de vies et en sauvera probablement des milliards d’autres.
Mais l’azote a une autre application : c’est l’ingrédient clé de l’explosif TNT (Trinitrotoluène). Dans son discours d’acceptation du prix Nobel, Haber n’a mentionné que la demande croissante de nourriture comme motivation, mais il était bien conscient de l’autre application de l’invention. Suite à sa découverte de la synthèse d’ammoniac, il avait passé la Première Guerre mondiale à travailler sur la recherche de gaz toxiques, ce qui lui avait valu le titre de « père de la guerre chimique ». L’invention de synthèse d’ammoniac de Haber va dans les deux sens ; il a contribué à sauver des millions de vies mais aussi à la mort de millions de personnes. Avancer de cent ans et même l’application positive de la synthèse d’ammoniac a des répercussions. Haber n’aurait pas pu prévoir « la cascade de changements environnementaux, y compris l’augmentation de la pollution de l’eau et de l’air, la perturbation des niveaux de gaz à effet de serre et la perte de biodiversité résultant de l’augmentation colossale de la production et de l’utilisation d’ammoniac qui devait s’ensuivre ». Cependant, la fertilisation azotée ne sera pas abandonnée de sitôt. La population mondiale devrait atteindre 9 milliards d’ici 2042 et accroître encore notre dépendance aux engrais azotés. Un certain nombre de scénarios différents pour l’utilisation future des engrais azotés et les défis susceptibles d’être rencontrés par ce que l’on a appelé « notre économie de l’azote » au cours des cent prochaines années sont discutés dans l’article « Comment un siècle de synthèse d’ammoniac a changé le monde » publié dans le numéro du 28 septembre 2008 de Nature Géoscience.
Qui voudrait vraiment juger si les avantages de l’invention de Haber l’emportent sur les répercussions ? Peut-on même envisager un avenir sans elle ? La synthèse d’ammoniac n’est pas isolée ; de nombreuses inventions ont eu des applications à la fois positives et négatives en plus de contribuer à la pollution de l’air, du sol et de l’eau. Les décideurs politiques, les chercheurs et les innovateurs se consacrent à trouver des technologies de lutte contre le changement climatique qui ne causeront pas de dommages supplémentaires à la planète.
https://www.thehindu.com/children/haber-ammonia-and-a-complex-legacy/article56832860.ece
https://www.wipo.int/wipo_magazine/en/2008/06/article_0011.html
