 Roux et Yersin, élèves de Pasteur, découvraient en 1888 que le bacille de là diphtérie n’agissait pas » en envahissant les tissus, mais par la diffusion dans l’organisme d’une substance toxique « , la toxine diphtérique. Behring et Kitasato identifièrent ensuite dans l’organisme des animaux infectés expérimentalement une substance antitoxique, un contre-poison à la toxine diphtérique, l’antitoxine. On sait également qu’au congrès tenu à Budapest, à l’automne de 1894, Emile Roux, Louis Martin et Chaillou apportent la révélation de la sérothérapie antidiphtérique. Ayant soumis des chevaux à des injections progressives de toxine diphtérique, ils avaient provoqué chez ceux-ci la formation d’antitoxines et utilisé leur sérum sanguin pour fournir à l’organisme des malades des moyens de défense qui lui faisaient défaut.
Roux et Yersin, élèves de Pasteur, découvraient en 1888 que le bacille de là diphtérie n’agissait pas » en envahissant les tissus, mais par la diffusion dans l’organisme d’une substance toxique « , la toxine diphtérique. Behring et Kitasato identifièrent ensuite dans l’organisme des animaux infectés expérimentalement une substance antitoxique, un contre-poison à la toxine diphtérique, l’antitoxine. On sait également qu’au congrès tenu à Budapest, à l’automne de 1894, Emile Roux, Louis Martin et Chaillou apportent la révélation de la sérothérapie antidiphtérique. Ayant soumis des chevaux à des injections progressives de toxine diphtérique, ils avaient provoqué chez ceux-ci la formation d’antitoxines et utilisé leur sérum sanguin pour fournir à l’organisme des malades des moyens de défense qui lui faisaient défaut.
 La diphtérie donne son nom
La diphtérie donne son nom La diphtérie, qui était auparavant appelée par une variété de noms, a obtenu son nom officiel du médecin français Pierre Bretonneau (1778-1862), qui a appelé la maladie diphtérite. L’origine était le mot grec pour «cuir» ou «peau», qui décrit le revêtement qui apparaît dans la gorge (c’est-à-dire la pseudomembrane). Bretonneau a également distingué la diphtérie de la scarlatine. Bretonneau a enregistré la première utilisation réussie de la trachéotomie dans un cas de diphtérie. Cette procédure, qui avait été utilisée pour traiter d’autres conditions, consiste à couper une ouverture dans la trachée et à insérer un tube à travers l’ouverture pour permettre le passage de l’air et l’élimination des sécrétions. Bretonneau avait tenté la procédure plusieurs fois auparavant, mais les patients sont décédés. Plus tard, un autre médecin français, Armand Trousseau (1801-1867), a montré un taux de survie d’environ 25% dans les trachéotomies qu’il a effectuées sur des personnes atteintes de diphtérie.
La diphtérie, qui était auparavant appelée par une variété de noms, a obtenu son nom officiel du médecin français Pierre Bretonneau (1778-1862), qui a appelé la maladie diphtérite. L’origine était le mot grec pour «cuir» ou «peau», qui décrit le revêtement qui apparaît dans la gorge (c’est-à-dire la pseudomembrane). Bretonneau a également distingué la diphtérie de la scarlatine. Bretonneau a enregistré la première utilisation réussie de la trachéotomie dans un cas de diphtérie. Cette procédure, qui avait été utilisée pour traiter d’autres conditions, consiste à couper une ouverture dans la trachée et à insérer un tube à travers l’ouverture pour permettre le passage de l’air et l’élimination des sécrétions. Bretonneau avait tenté la procédure plusieurs fois auparavant, mais les patients sont décédés. Plus tard, un autre médecin français, Armand Trousseau (1801-1867), a montré un taux de survie d’environ 25% dans les trachéotomies qu’il a effectuées sur des personnes atteintes de diphtérie. Un remède contre la diphtérie, 1894
Un remède contre la diphtérie, 1894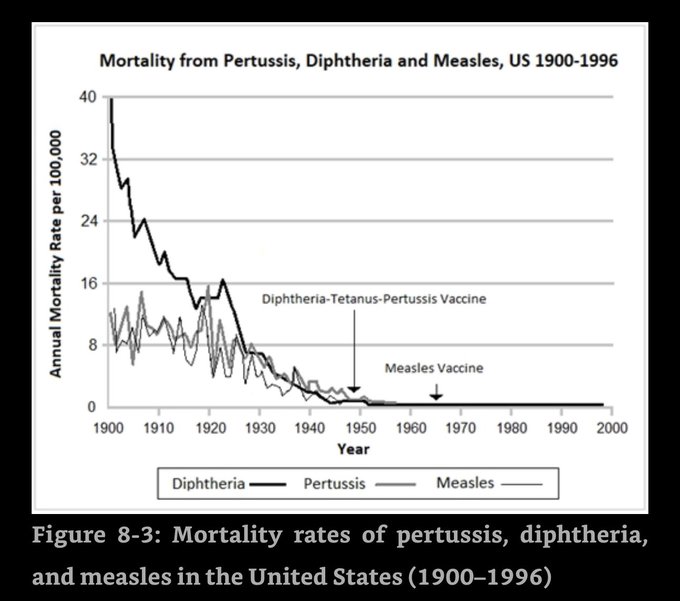



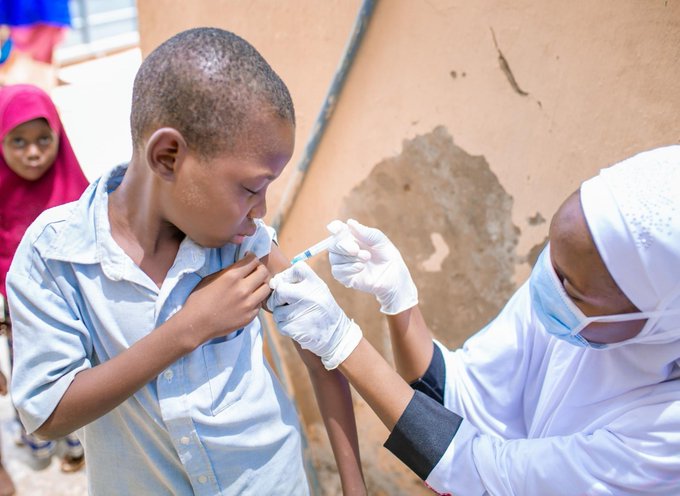
 Le vaccin d’aujourd’hui, recommandé pour tous les nourrissons et pour les adultes qui n’ont pas été immunisés, est fabriqué en traitant la toxine diphtérique avec de la chaleur et des produits chimiques, détruisant sa capacité à produire des maladies mais lui permettant de stimuler la production d’anticorps. Parce que le vaccin est si efficace et si largement utilisé, la diphtérie est rare dans les pays industrialisés, mais lorsqu’elle survient, elle peut être traitée avec de l’antitoxine diphtérique. Aux États-Unis, le médicament n’est disponible que par l’intermédiaire des Centers for Disease Control and Prevention, qui l’importent du Brésil, l’un des rares pays au monde à le fabriquer encore.
Le vaccin d’aujourd’hui, recommandé pour tous les nourrissons et pour les adultes qui n’ont pas été immunisés, est fabriqué en traitant la toxine diphtérique avec de la chaleur et des produits chimiques, détruisant sa capacité à produire des maladies mais lui permettant de stimuler la production d’anticorps. Parce que le vaccin est si efficace et si largement utilisé, la diphtérie est rare dans les pays industrialisés, mais lorsqu’elle survient, elle peut être traitée avec de l’antitoxine diphtérique. Aux États-Unis, le médicament n’est disponible que par l’intermédiaire des Centers for Disease Control and Prevention, qui l’importent du Brésil, l’un des rares pays au monde à le fabriquer encore.
Évolution de l’écosystème pharmaceutique-biotechnologique et choix de carrière 
 Ces leçons n’ont pas été perdues pour l’industrie pharmaceutique. Ce changement n’a pas été catalysé par une menace concurrentielle mais par l’impact potentiel de la révolution génomique/protéomique sur le processus de découverte de médicaments. Les principales sociétés pharmaceutiques ont réalisé les implications de ce changement technologique : un nombre croissant de nouvelles cibles médicamenteuses et le potentiel de développement d’agents thérapeutiques pour des maladies jusqu’alors inattaquables.
Ces leçons n’ont pas été perdues pour l’industrie pharmaceutique. Ce changement n’a pas été catalysé par une menace concurrentielle mais par l’impact potentiel de la révolution génomique/protéomique sur le processus de découverte de médicaments. Les principales sociétés pharmaceutiques ont réalisé les implications de ce changement technologique : un nombre croissant de nouvelles cibles médicamenteuses et le potentiel de développement d’agents thérapeutiques pour des maladies jusqu’alors inattaquables.  Les grandes sociétés pharmaceutiques se sont alliées à des entreprises de biotechnologie émergentes qui, en échange d’un soutien financier, ont fourni de nouvelles technologies et capacités pour améliorer le processus de découverte de médicaments des grandes sociétés pharmaceutiques. D’autres facteurs accélérant le changement étaient le coût croissant du développement de médicaments et l’augmentation des coûts des médicaments sur ordonnance qui ont conduit à une industrie de fabrication de médicaments génériques plus forte. La « menace générique » a eu un impact significatif sur l’industrie pharmaceutique, incitant les grandes entreprises pharmaceutiques à se concentrer sur leurs principales capacités : construire un pipeline de médicaments robuste, obtenir une approbation réglementaire rapide des médicaments et une commercialisation rapide sur le marché mondial. L’accent croissant mis sur ces compétences de base a ouvert des opportunités à d’autres entreprises spécialisées pour participer à l’écosystème américain de la biotechnologie pharmaceutique (PBE).
Les grandes sociétés pharmaceutiques se sont alliées à des entreprises de biotechnologie émergentes qui, en échange d’un soutien financier, ont fourni de nouvelles technologies et capacités pour améliorer le processus de découverte de médicaments des grandes sociétés pharmaceutiques. D’autres facteurs accélérant le changement étaient le coût croissant du développement de médicaments et l’augmentation des coûts des médicaments sur ordonnance qui ont conduit à une industrie de fabrication de médicaments génériques plus forte. La « menace générique » a eu un impact significatif sur l’industrie pharmaceutique, incitant les grandes entreprises pharmaceutiques à se concentrer sur leurs principales capacités : construire un pipeline de médicaments robuste, obtenir une approbation réglementaire rapide des médicaments et une commercialisation rapide sur le marché mondial. L’accent croissant mis sur ces compétences de base a ouvert des opportunités à d’autres entreprises spécialisées pour participer à l’écosystème américain de la biotechnologie pharmaceutique (PBE).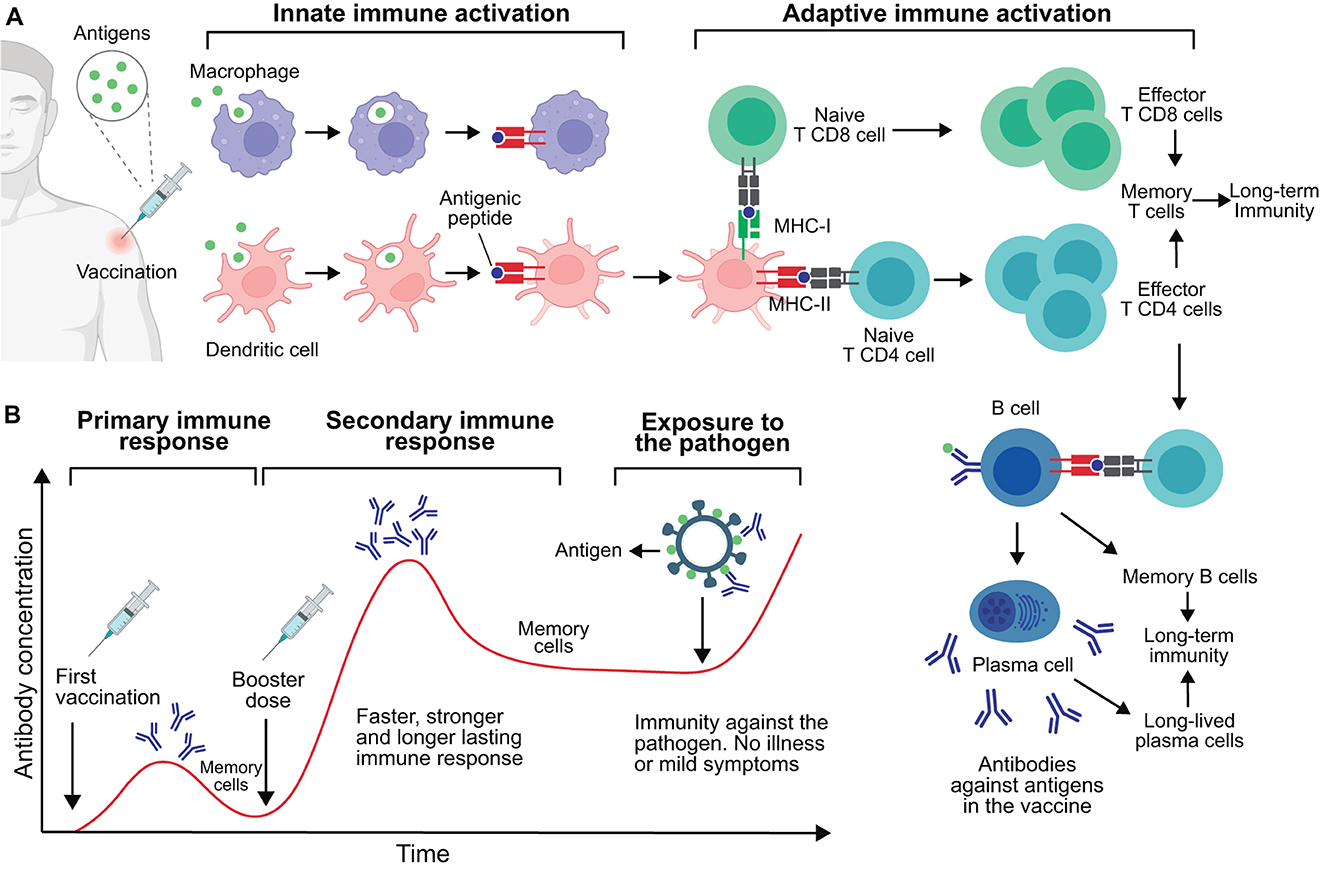 Big pharma : passé des chaînes d’approvisionnement aux écosystèmes Les États-Unis sont le marché pharmaceutique le plus vaste et le plus compétitif au monde. Elle compte le plus grand nombre d’employés et d’entreprises qui soutiennent cette industrie. Les fabricants de médicaments étrangers, comme Novartis et d’autres, transfèrent une plus grande partie de leurs recherches aux États-Unis et s’insèrent dans ce PBE dynamique dont l’objectif est défini par les grandes sociétés pharmaceutiques pour augmenter la vitesse et la productivité du processus de développement de médicaments.
Big pharma : passé des chaînes d’approvisionnement aux écosystèmes Les États-Unis sont le marché pharmaceutique le plus vaste et le plus compétitif au monde. Elle compte le plus grand nombre d’employés et d’entreprises qui soutiennent cette industrie. Les fabricants de médicaments étrangers, comme Novartis et d’autres, transfèrent une plus grande partie de leurs recherches aux États-Unis et s’insèrent dans ce PBE dynamique dont l’objectif est défini par les grandes sociétés pharmaceutiques pour augmenter la vitesse et la productivité du processus de développement de médicaments.  Le concept d’écosystème4 offre un contexte plus riche que les modèles de chaîne d’approvisionnement établis, car le PBE est un environnement dynamique et en croissance. Les membres peuvent utiliser le financement des grandes sociétés pharmaceutiques pour créer des entreprises susceptibles de concurrencer les entreprises établies. Millennium Pharmaceuticals incarne une entreprise qui atteint cet objectif. En revanche, les membres des chaînes d’approvisionnement des entreprises allégées sont réticents à défier « l’assembleur/intégrateur ». Cette différence reflète les changements de flux au sein du système. Pour l’industrie automobile, il s’agit de composants/ensembles intégrés, alors que dans le PBE, il s’agit des connaissances nécessaires au développement rentable de nouveaux agents thérapeutiques.
Le concept d’écosystème4 offre un contexte plus riche que les modèles de chaîne d’approvisionnement établis, car le PBE est un environnement dynamique et en croissance. Les membres peuvent utiliser le financement des grandes sociétés pharmaceutiques pour créer des entreprises susceptibles de concurrencer les entreprises établies. Millennium Pharmaceuticals incarne une entreprise qui atteint cet objectif. En revanche, les membres des chaînes d’approvisionnement des entreprises allégées sont réticents à défier « l’assembleur/intégrateur ». Cette différence reflète les changements de flux au sein du système. Pour l’industrie automobile, il s’agit de composants/ensembles intégrés, alors que dans le PBE, il s’agit des connaissances nécessaires au développement rentable de nouveaux agents thérapeutiques.
 Les grandes sociétés pharmaceutiques sont alimentées par des réseaux de fournisseurs organisés en niveaux, un peu comme les réseaux de fournisseurs de l’industrie automobile.5 Plus l’impact de la valeur des biens ou des services sur le produit/service final est direct, plus le niveau est élevé (ou inférieur numéro du niveau) dans l’écosystème. — Les fournisseurs de niveau 1 fournissent aux grandes sociétés pharmaceutiques des connaissances, du matériel ou des services qui ont un impact direct sur la valeur et la productivité du processus de développement de médicaments. — Les fournisseurs de niveau 2 sont les fabricants d’outils qui fournissent les réactifs, l’instrumentation/les systèmes intégrés ou les animaux nécessaires aux membres de ce réseau pour effectuer efficacement la science nécessaire au développement de nouveaux médicaments.
Les grandes sociétés pharmaceutiques sont alimentées par des réseaux de fournisseurs organisés en niveaux, un peu comme les réseaux de fournisseurs de l’industrie automobile.5 Plus l’impact de la valeur des biens ou des services sur le produit/service final est direct, plus le niveau est élevé (ou inférieur numéro du niveau) dans l’écosystème. — Les fournisseurs de niveau 1 fournissent aux grandes sociétés pharmaceutiques des connaissances, du matériel ou des services qui ont un impact direct sur la valeur et la productivité du processus de développement de médicaments. — Les fournisseurs de niveau 2 sont les fabricants d’outils qui fournissent les réactifs, l’instrumentation/les systèmes intégrés ou les animaux nécessaires aux membres de ce réseau pour effectuer efficacement la science nécessaire au développement de nouveaux médicaments. Le tableau 1 donne des exemples d’entreprises à chaque niveau du réseau. Veuillez noter que les entreprises des deux niveaux élargissent souvent leurs modèles commerciaux pour fournir des produits et services supplémentaires qui profitent au PBE. Cette catégorisation est à titre indicatif seulement et ne représente pas l’étendue des produits/services que ces entreprises offrent au PBE.
Le tableau 1 donne des exemples d’entreprises à chaque niveau du réseau. Veuillez noter que les entreprises des deux niveaux élargissent souvent leurs modèles commerciaux pour fournir des produits et services supplémentaires qui profitent au PBE. Cette catégorisation est à titre indicatif seulement et ne représente pas l’étendue des produits/services que ces entreprises offrent au PBE. La position des entreprises dans le PBE peut changer au fil du temps en fonction de la valeur qu’elles apportent aux grandes sociétés pharmaceutiques. Par exemple, au milieu des années 1990, les entreprises axées sur la chimie combinatoire ou les technologies utilisées pour identifier rapidement de nouvelles cibles médicamenteuses étaient les chouchous de la communauté des investisseurs. La justification de cette valeur était basée sur la conviction que la fusion de la sortie des deux technologies dans des procédures de dépistage à haut débit conduirait à une augmentation spectaculaire des cibles médicamenteuses potentielles. Cependant, un récent article en première page du Wall Street Journal a montré que cette approche s’est avérée inefficace pour générer de nouveaux médicaments.6 On a estimé qu’un seul nouveau médicament a été développé à partir de bibliothèques de chimie combinatoire. La valeur du niveau 1 a migré vers les sociétés de biotechnologie qui ont des candidats-médicaments à un stade précoce.7 La raison de la migration de la valeur est claire : le développement de nouveaux candidats-médicaments est aligné sur le besoin des grandes sociétés pharmaceutiques de disposer d’un solide portefeuille de produits.
La position des entreprises dans le PBE peut changer au fil du temps en fonction de la valeur qu’elles apportent aux grandes sociétés pharmaceutiques. Par exemple, au milieu des années 1990, les entreprises axées sur la chimie combinatoire ou les technologies utilisées pour identifier rapidement de nouvelles cibles médicamenteuses étaient les chouchous de la communauté des investisseurs. La justification de cette valeur était basée sur la conviction que la fusion de la sortie des deux technologies dans des procédures de dépistage à haut débit conduirait à une augmentation spectaculaire des cibles médicamenteuses potentielles. Cependant, un récent article en première page du Wall Street Journal a montré que cette approche s’est avérée inefficace pour générer de nouveaux médicaments.6 On a estimé qu’un seul nouveau médicament a été développé à partir de bibliothèques de chimie combinatoire. La valeur du niveau 1 a migré vers les sociétés de biotechnologie qui ont des candidats-médicaments à un stade précoce.7 La raison de la migration de la valeur est claire : le développement de nouveaux candidats-médicaments est aligné sur le besoin des grandes sociétés pharmaceutiques de disposer d’un solide portefeuille de produits.
 Se préparer à une carrière dans l’écosystème pharmaceutique et biotechnologique
Se préparer à une carrière dans l’écosystème pharmaceutique et biotechnologique
Que signifie ce qui précède pour les diplômés universitaires qui souhaitent une carrière épanouissante dans des entreprises du PBE américain ? En tant que futurs employés de cette industrie, les diplômés doivent prendre à cœur les leçons de l’écosystème.
Tout d’abord, augmentez la valeur de vos compétences afin qu’elles puissent profiter à vous et à votre employeur. Pour les nouveaux diplômés, cela signifie aller à l’école doctorale et se former dans des laboratoires avec des environnements intellectuellement stimulants. Si ce cours n’est pas pour vous, commencez par travailler comme technicien dans un laboratoire de recherche universitaire avec le même environnement difficile. Dans les deux cas, apprenez tout ce que vous pouvez avec le temps dont vous disposez. Vous seul bénéficierez de cet effort. Deuxièmement, comprendre la dynamique des changements de valeur dans le PBE. Ceci est essentiel non seulement pour développer les compétences nécessaires dans l’écosystème, mais aussi pour augmenter votre connaissance des entreprises qui correspondent à vos objectifs et aspirations. La meilleure façon d’améliorer votre compréhension de ces changements est de commencer à développer un intérêt pour la gestion de la technologie. De nouveaux concepts tels que la technologie de rupture10, 11 et l’innovation ouverte12 changent la façon dont les entreprises établies développent de nouveaux produits.
Troisièmement, engagez le dialogue avec d’autres personnes plus expérimentées que vous dans ce domaine. Il a été estimé que 40 États différents ont des initiatives significatives en matière de biotechnologie. Découvrez comment vous pouvez interagir avec des scientifiques et des hommes d’affaires férus de technologie dans ce groupe.
L’évolution de la biotechnologie et son impact sur les soins de santé
Depuis plus de trois décennies, le domaine de la biotechnologie a eu un impact extraordinaire sur la science, les soins de santé, le droit, l’environnement réglementaire et les affaires. Au cours de cette période, plus de 260 nouveaux produits biotechnologiques ont été approuvés pour plus de 230 indications. Les ventes mondiales de ces produits ont dépassé 175 milliards de dollars en 2013 et ont contribué à soutenir un secteur dynamique des sciences de la vie qui comprend plus de 4 600 sociétés de biotechnologie dans le monde. Dans cet article, nous examinons l’évolution de la biotechnologie au cours des trois dernières décennies et l’impact profond qu’elle a eu sur les soins de santé à travers quatre voies interdépendantes et interdépendantes : les innovations scientifiques, l’activité gouvernementale, le développement des entreprises et les soins aux patients. L’impact futur de la biotechnologie est prometteur, tant que les secteurs public et privé continueront de promouvoir des politiques et de fournir des fonds qui mènent à des percées scientifiques ; les gouvernements continuent d’offrir des incitations à l’innovation biotechnologique du secteur privé ; l’industrie développe des modèles commerciaux pour une recherche et un développement rentables ; et toutes les parties prenantes établissent des politiques pour s’assurer que les progrès thérapeutiques qui atténuent ou guérissent les conditions médicales qui ont actuellement des traitements inadéquats ou inexistants sont accessibles au public à un coût raisonnable.
Biotechnologie : un aperçu
Traditionnellement, la plupart des médicaments pour les maladies humaines étaient des médicaments à petites molécules (chimiques) fabriqués par des sociétés pharmaceutiques bien établies. À partir des années 1980, de petites entreprises de biotechnologie en démarrage ont commencé à mener des recherches sur des médicaments à grandes molécules (biologiques) basés sur ou fabriqués à partir de tissus biologiques. Les produits biologiques sont désormais au centre des préoccupations des sociétés pharmaceutiques et biotechnologiques en termes de recherche et développement (R&D) et de vente de produits. Nous appelons ce secteur biopharmaceutique. En 2013, les ventes mondiales de produits biotechnologiques ont dépassé 175 milliards de dollars, soit environ 19 % des 950 milliards de dollars de ventes totales de produits sur ordonnance dans le monde. Parmi les dix principaux produits pharmaceutiques et biotechnologiques en termes de ventes, sept étaient ces derniers. De plus, sur les 124 médicaments sur ordonnance considérés comme des blockbusters (définis comme ayant des ventes annuelles de 1 milliard de dollars ou plus) en 2013, 47 (38 %) étaient des produits biotechnologiques.
L’annexe 2 répertorie les produits biotechnologiques et les produits vedettes dont la vente est approuvée aux États-Unis par la Food and Drug Administration (FDA) et développés par vingt-quatre entreprises qui ont au moins trois produits biotechnologiques commercialisés aux États-Unis. Presque tous les domaines thérapeu-tiques sont représentés, l’oncologie, la rhumatologie, le diabète, l’hématologie, la neurologie et les maladies infectieuses étant les principaux domaines en termes de ventes. Le tableau énumère le nombre de produits biotechnologiques développés dans quinze disciplines médicales au cours des trois périodes d’étude….
La naissance de la biotechnologie (1980–89)
Innovations scientifiques
Les travaux pionniers en biotechnologie remontent au milieu des années 1970. Cependant, l’évolution de l’industrie biotechnologique telle qu’elle est connue aujourd’hui a commencé dans les années 1980, avec des innovations scientifiques menant à la commercialisation de produits biotechnologiques. La preuve de principe pour la découverte et le développement de produits a été établie pour les protéines d’ADN recombinant, les anticorps monoclonaux et les vaccins. Pour la première fois, des protéines recombinantes ont été utilisées pour traiter des maladies débilitantes majeures, telles que le diabète, l’anémie et le retard de croissance, maladies dont une carence en protéines était responsable.
La commercialisation de traitements efficaces a nécessité trois grandes étapes. Premièrement, les protéines responsables devaient être isolées, identifiées, séquencées et clonées dans des cellules hôtes non humaines. Deuxièmement, des techniques de production à grande échelle étaient nécessaires pour produire des traitements en quantités et d’une qualité suffisante pour la commercialisation. Et troisièmement, de nouvelles analyses de processus complexes étaient nécessaires pour garantir la qualité et la cohérence des produits.
Des vaccins tels que le vaccin contre l’antigène de l’hépatite ont également été développés en utilisant la technologie de l’ADN recombinant. Dans ce processus, un antigène protéique a été identifié, fabriqué, puis incorporé dans une formulation de vaccin. La technologie des anticorps monoclonaux a commencé avec le développement de cellules d’hybridome (la fusion d’une cellule plasmatique et d’une cellule de myélome multiple). Ces cellules d’hybridome avaient la capacité de produire les anticorps monoclonaux spécifiques de l’antigène ciblé en grandes quantités. En outre, un processus à grande échelle a été créé pour que les hybridomes fabriquent suffisamment d’un produit donné pour la commercialisation.
https://www.science.org/content/article/evolution-pharmaceutical-biotech-ecosystem-and-career-choice
https://www.nytimes.com/2010/05/11/health/11first.html