 Julius Lothar Meyer – Inventeur de la loi périodique
Julius Lothar Meyer – Inventeur de la loi périodique Professeur Lothar Meyer (1830-1895)
Professeur Lothar Meyer (1830-1895) Julius Lothar Meyer : Pourquoi sa découverte est si importante
Julius Lothar Meyer : Pourquoi sa découverte est si importante
 Julius Lothar Meyer – Inventeur de la loi périodique
Julius Lothar Meyer – Inventeur de la loi périodique Le 19 août 1830 , le chimiste allemand Julius Lothar Meyer est né. Meyer a été l’un des pionniers dans l’élaboration du premier tableau périodique des éléments chimiques . Il découvre la loi périodique , indépendamment de Dmitri Mendeleïev , à peu près à la même époque ( 1869 ). Cependant, il n’a pas développé la classification périodique des éléments chimiques aussi complètement que Mendeleïev .
Le 19 août 1830 , le chimiste allemand Julius Lothar Meyer est né. Meyer a été l’un des pionniers dans l’élaboration du premier tableau périodique des éléments chimiques . Il découvre la loi périodique , indépendamment de Dmitri Mendeleïev , à peu près à la même époque ( 1869 ). Cependant, il n’a pas développé la classification périodique des éléments chimiques aussi complètement que Mendeleïev . « Que les éléments chimiques encore indivis soient des substances absolument irréductibles, est actuellement au moins très improbable. Il semble plutôt que les atomes des éléments ne soient pas les constituants finaux, mais seulement les constituants immédiats des molécules des éléments et des composés – le Molekeln ou molécule comme principale division de la matière, les atomes étant considérés comme du second ordre, à leur tour. constitué de particules de matière d’un troisième ordre supérieur.
« Que les éléments chimiques encore indivis soient des substances absolument irréductibles, est actuellement au moins très improbable. Il semble plutôt que les atomes des éléments ne soient pas les constituants finaux, mais seulement les constituants immédiats des molécules des éléments et des composés – le Molekeln ou molécule comme principale division de la matière, les atomes étant considérés comme du second ordre, à leur tour. constitué de particules de matière d’un troisième ordre supérieur.
– Lothar Meyer, spéculant en 1870, sur l’existence de particules subatomiques,  Julius Lothar Meyer – Petite enfance
Julius Lothar Meyer – Petite enfance Julius Lothar Meyer est né à Varel , en Allemagne (qui faisait alors partie du duché d’Oldenbourg ), en tant que fils de Friedrich August Meyer, médecin, et d’Anna Biermann. Après avoir fréquenté l’Altes Gymnasium d’Oldenbourg, il étudie la médecine à l’ Université de Zurich en 1851. Il étudie auprès de Carl Ludwig, ce qui le pousse à consacrer son attention également à la chimie physiologique. En 1853, il est allé à l’ Université de Würzburg , où il a étudié la pathologie , en tant qu’étudiant du célèbre médecin prussien Rudolf Virchow .
Julius Lothar Meyer est né à Varel , en Allemagne (qui faisait alors partie du duché d’Oldenbourg ), en tant que fils de Friedrich August Meyer, médecin, et d’Anna Biermann. Après avoir fréquenté l’Altes Gymnasium d’Oldenbourg, il étudie la médecine à l’ Université de Zurich en 1851. Il étudie auprès de Carl Ludwig, ce qui le pousse à consacrer son attention également à la chimie physiologique. En 1853, il est allé à l’ Université de Würzburg , où il a étudié la pathologie , en tant qu’étudiant du célèbre médecin prussien Rudolf Virchow .  Après avoir obtenu son diplôme de médecine de Würzburg en 1854, il est allé à Heidelberg, où Robert Bunsen a occupé la chaire. de chimie. De là, il a émigré à Königsberg , où il est resté jusqu’en 1858. À Königsberg, ses études ont été consacrées principalement à la physique mathématique sous la direction du minéralogiste, physicien et mathématicien Franz Ernst Neumann . Il y poursuivit également ses intérêts physiologiques antérieurs en étudiant l’effet du monoxyde de carbone sur le sang. En 1858, il obtient un doctorat. à Breslau avec une thèse sur l’action du monoxyde de carbone sur le sang. Avec cet intérêt pour la physiologie de la respiration, il avait reconnu que l’oxygène se combine avec l’ hémoglobine dans le sang.
Après avoir obtenu son diplôme de médecine de Würzburg en 1854, il est allé à Heidelberg, où Robert Bunsen a occupé la chaire. de chimie. De là, il a émigré à Königsberg , où il est resté jusqu’en 1858. À Königsberg, ses études ont été consacrées principalement à la physique mathématique sous la direction du minéralogiste, physicien et mathématicien Franz Ernst Neumann . Il y poursuivit également ses intérêts physiologiques antérieurs en étudiant l’effet du monoxyde de carbone sur le sang. En 1858, il obtient un doctorat. à Breslau avec une thèse sur l’action du monoxyde de carbone sur le sang. Avec cet intérêt pour la physiologie de la respiration, il avait reconnu que l’oxygène se combine avec l’ hémoglobine dans le sang.
Classification périodique des éléments chimiques
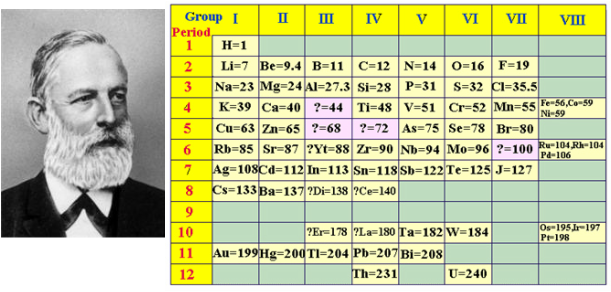
En 1859, il devient Privatdozent en physique et chimie à l’Université de Breslau. En 1866, Meyer accepta un poste à l’Académie forestière d’Eberswalde à Neustadt-Eberswalde , où il resta jusqu’en 1868, date à laquelle il se rendit au Polytechnikum de Karlsruhe pour être nommé professeur. Meyer est surtout connu pour son rôle dans la classification périodique des éléments chimiques . Il a noté, comme JAR Newlands l’a fait en Angleterre, que si chaque élément est rangé dans l’ordre de son poids atomique , il tombe dans des groupes de propriétés chimiques et physiques similaires répétés à intervalles périodiques. Selon lui, si les poids atomiques étaient portés en ordonnées et les volumes atomiques en abscisses— la courbe obtenait une série de maxima et de minima — les éléments les plus électropositifs apparaissant aux sommets de la courbe dans l’ordre de leurs poids atomiques.
Dimitri Mendeleïev
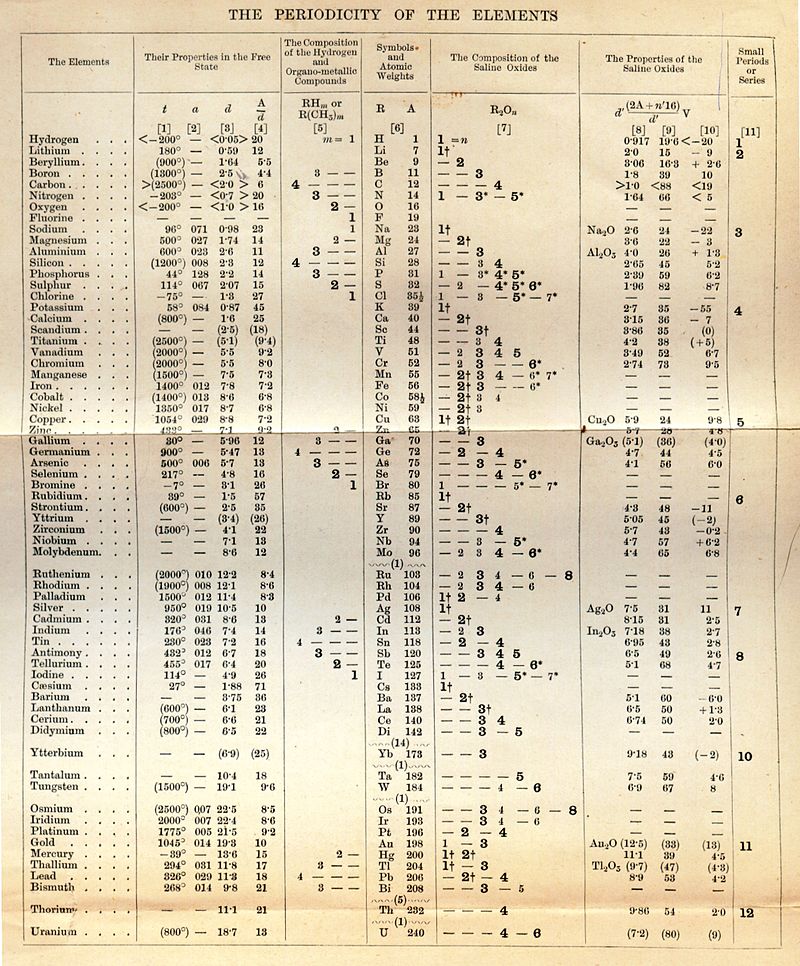
Son livre, Die modernen Theorien der Chemie , qu’il commença à écrire à Breslau en 1862 et qui fut publié en 1864, contenait une première version du tableau périodique contenant 28 éléments, classant les éléments en six familles selon leur valence — pour la première fois, les éléments avaient été regroupés en fonction de leur valence, un nombre appelé le pouvoir de combinaison de chaque élément pour relier une famille particulière.[4] Le manuel a connu cinq éditions et a été traduit en anglais, français et russe. Les travaux sur l’organisation des éléments par poids atomique, jusque-là, avaient été bloqués par des mesures inexactes des poids atomiques. En 1869, Dmitri Mendeleïevpublié un tableau périodique de tous les éléments connus [2]. Quelques mois plus tard, Meyer a publié indépendamment une version révisée et élargie de son tableau de 1864, qui était similaire à celui publié par Mendeleev et un article montrant graphiquement la périodicité des éléments en fonction du poids atomique. Meyer, ainsi que d’autres chimistes, doutaient de la loi périodique de Mendeleïev, et il a critiqué Mendeleïev pour « changer les poids atomiques des éléments existants, uniquement en ce qui concerne la possibilité d’une loi périodique dans sa structure ». Cependant, le travail de Mendeleev a reçu un soutien important, lorsque les nouveaux éléments ont été trouvés comme prévu et les poids atomiques en conséquence. En 1882, Meyer et Mendeleev ont reçu la médaille Davy de la Royal Societyen reconnaissance de leur travail sur la loi périodique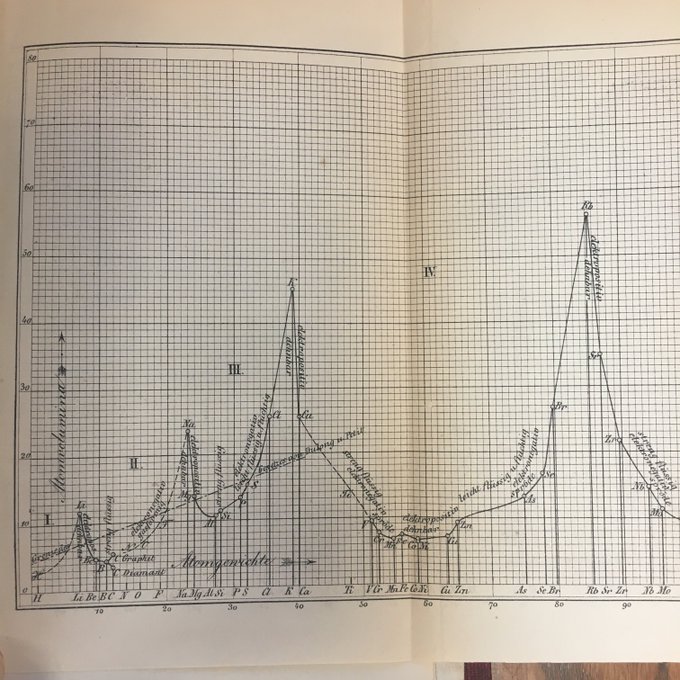
Même aujourd’hui, au XXIe siècle, bien que les historiens reconnaissent que d’autres, en particulier Meyer, devraient recevoir un crédit considérable pour la découverte des propriétés périodiques des éléments, la plupart des manuels ne créditent que Mendeleïev.
Professeur Lothar Meyer (1830-1895) JULIUS LOTHAR MEYER est né à Varel à Oldenbourg, le 19 août 1830. Après avoir terminé ses études au Gymnasium. il étudie à l’Université de Zurich de 1851 à 1853, puis à Würzburg de 1853 à 1854 ; de Wurzburg, il se rendit à Heidelberg, où il resta jusqu’à l’automne 1856, et de là il émigra à Königsberg, où il resta jusqu’à Pâques 1858. L’intention initiale de Meyer était de se consacrer à la médecine, et il obtint son diplôme de docteur en médecine à Wurzburg. le 24 février 1854. A Heidelberg, il subit l’influence de Buiisen et son travail devient de plus en plus chimique. A Königsberg, ses études furent consacrées principalement à la physique mathématique, sous la direction de F. Neumann. En 1858, il a obtenu le diplôme de doctorat. à Breslau; et le 21 février 1859, il reçut un congé pour enseigner la chimie et la physique. De 1859 à 1866, Meyer était responsable du laboratoire de chimie de l’Institut physiologique de Breslau. En 1866, il fut appelé à la Royal Prussian Forstakademie à Eberswalde, où il resta jusqu’en 1868, date à laquelle il se rendit au Polytechnikum de Carlsruhe.
JULIUS LOTHAR MEYER est né à Varel à Oldenbourg, le 19 août 1830. Après avoir terminé ses études au Gymnasium. il étudie à l’Université de Zurich de 1851 à 1853, puis à Würzburg de 1853 à 1854 ; de Wurzburg, il se rendit à Heidelberg, où il resta jusqu’à l’automne 1856, et de là il émigra à Königsberg, où il resta jusqu’à Pâques 1858. L’intention initiale de Meyer était de se consacrer à la médecine, et il obtint son diplôme de docteur en médecine à Wurzburg. le 24 février 1854. A Heidelberg, il subit l’influence de Buiisen et son travail devient de plus en plus chimique. A Königsberg, ses études furent consacrées principalement à la physique mathématique, sous la direction de F. Neumann. En 1858, il a obtenu le diplôme de doctorat. à Breslau; et le 21 février 1859, il reçut un congé pour enseigner la chimie et la physique. De 1859 à 1866, Meyer était responsable du laboratoire de chimie de l’Institut physiologique de Breslau. En 1866, il fut appelé à la Royal Prussian Forstakademie à Eberswalde, où il resta jusqu’en 1868, date à laquelle il se rendit au Polytechnikum de Carlsruhe.
En 1876, le professeur Fittig fut appelé de Tübingen à l’Université de Strasbourg et Lothar Meyer fut nommé pour occuper le poste vacant à Tübingen. Il avait presque vingt ans de travail à Tübingen quand la sommation arriva. L’apoplexie cérébrale a arrêté ses travaux, le 12 avril de cette année ; et, plotzlich, 8anft, und schmerzlos, il passa. C’est alors qu’il enseigne la chimie et la physique à Breslau que Meyer publie la première édition de l’ouvrage sur lequel repose principalement sa réputation de chimiste philosophe. « Die Moderiien Theorien del’ Chemie » paraît en 1864. Une deuxième édition a été publiée en 1872; et depuis lors ont paru une troisième, quatrième et cinquième édition. Au moment de sa mort, Meyer était engagé dans la préparation d’une sixième édition, qu’il avait l’intention de publier en trois parties plus ou moins indépendantes. Une traduction anglaise de la cinquième édition, par MM. Bedson et Williams, parut en 1888. En 1883, les professeurs. Meyer et Seubert ont recalculé les poids atomiques des éléments à partir des données originales et ont rendu hommage à tous les chimistes en publiant leurs résultats, sous le titre « Die Atomgewichte der Elemente aus den Originalzahlen neu berechnet ». Lothar Meyer a été l’un des premiers chercheurs des relations entre les propriétés et les poids atomiques des éléments.  Dans la première édition de ses « 44 Modernen Theorien » (publiée en 1864), il a tracé les relations entre les poids atomiques et les valeurs hémiques des éléments ; et en décembre 1869 parut un mémoire de lui intitulé « Die Natur der chemischen Elemente als Funktion ihrer Atomgewichte », dans lequel il classa les éléments par ordre de poids atomique, dans un seul tableau, et indiqua le caractère périodique de la dépendance des propriétés sur poids atomiques. L’énonciation claire, et l’application en détail, de la généralisation la plus ambitieuse qui ait été faite en chimie depuis les travaux de Dalton, doit, sans aucun doute, être attribuée à ce grand chimiste Mende- leeff, mais, néanmoins, une lecture de la La controverse entre Mendeleeff et Meyer montre, je pense, que Meyer est arrivé à la conception fondamentale. de la loi périodique indépendamment de Mendeleeff. Ceux qui s’intéressent à de telles controverses trouveront des articles de Mendeleeff et Meyer dans Berichte xiii, pp. 259, 1796, 2043 [1880].
Dans la première édition de ses « 44 Modernen Theorien » (publiée en 1864), il a tracé les relations entre les poids atomiques et les valeurs hémiques des éléments ; et en décembre 1869 parut un mémoire de lui intitulé « Die Natur der chemischen Elemente als Funktion ihrer Atomgewichte », dans lequel il classa les éléments par ordre de poids atomique, dans un seul tableau, et indiqua le caractère périodique de la dépendance des propriétés sur poids atomiques. L’énonciation claire, et l’application en détail, de la généralisation la plus ambitieuse qui ait été faite en chimie depuis les travaux de Dalton, doit, sans aucun doute, être attribuée à ce grand chimiste Mende- leeff, mais, néanmoins, une lecture de la La controverse entre Mendeleeff et Meyer montre, je pense, que Meyer est arrivé à la conception fondamentale. de la loi périodique indépendamment de Mendeleeff. Ceux qui s’intéressent à de telles controverses trouveront des articles de Mendeleeff et Meyer dans Berichte xiii, pp. 259, 1796, 2043 [1880].
Dans son discours à la Société chimique allemande du 29 mai 1893, « Ueber den Vortrag der unorganischen Ohemie nach dem naturliehen Systeme der Elemente », Meyer cite les mots que Laurent avait employés cinquante ans auparavant à propos de la chimie organique, et les applique à la enseignement de la chimie inorganique à l’heure actuelle : Que l’arbitraire yrégne sans partage. Si ces mots s’appliquent aujourd’hui à l’enseignement de la chimie inorganique et générale, combien plus complètement et littéralement étaient-ils applicables à l’époque où parut il y a trente ans la première édition des « Die Modernen Theorien » de Meyer ! Ce livre a probablement fait plus que toute autre publication dans les vingt années qui ont suivi 1861 pour faire avancer l’étude de la chimie comparée ; son influence sur la conception de la chimie en tant qu’ensemble précis et ordonné de faits et de principes a été très grande et tout à fait bonne. 
Ainsi Lothar Meyer a été amené à consacrer une grande quantité de travail à la tâche quelque peu ingrate de recalculer toutes ces valeurs ; le résultat de ce travail, réalisé avec l’aide de son collègue le Prof. Seubert, parut en 1883. Ce travail reçut une valeur supplémentaire du fait qu’il parut presque en même temps que la « Reealculation of the Atomic Weights » de Clarke. .” Chaque travailleur de ce département a les données de tous les travailleurs précédents sous la main et présentées sous la forme la plus gérable. Outre ces deux traités portant sur la chimie générale, Lothar Meyer était chercheur dans le domaine de la chimie expérimentale. Il a publié des mémoires de sous-j eets dans presque toutes les branches de la science ; sur le poids atomique du béryllium, sur les déterminations des densités de vapeur, sur la combustion du monoxyde de carbone, sur la préparation de l’acide iodhydrique, sur le transport des gaz, de l’huile, de divers composés organiques et sur d’autres matières. Un grand chimiste nous a quittés ; son œuvre demeure, et cette œuvre restera à jamais en mémoire. MM PATTISON MUIR. sur le t ransp i rat ion de gaz, d’huile divers composés organiques, et sur d’autres matières. Un grand chimiste nous a quittés ; son œuvre demeure, et cette œuvre restera à jamais en mémoire. MM PATTISON MUIR. sur le t ransp i rat ion de gaz, d’huile divers composés organiques, et sur d’autres matières. Un grand chimiste nous a quittés ; son œuvre demeure, et cette œuvre restera à jamais en mémoire. MM PATTISON MUIR.
Julius Lothar Meyer : Pourquoi sa découverte est si importante
C’est la journée de Julius Lothar Meyer pour briller. Le scientifique, l’un des deux à créer indépendamment un tableau périodique moderne, repose souvent dans l’ombre historique de Dmitri Mendeleïev. Mais Meyer, qui a été mis en évidence aujourd’hui, a d’abord créé un système critique. Plus tard, il a fait des progrès qui jouent sur la façon dont les tableaux périodiques sont perçus aujourd’hui. Une époque de grands bouleversements – Meyer et Mendeleïev partagent plus qu’une quête commune. Les deux partageaient en fait le même professeur – Robert Busen, lui-même célèbre – à l’Université de Heidelberg à seulement cinq ans d’intervalle. En 1860, les deux jeunes scientifiques ont tous deux assisté au tout premier rassemblement international de chimistes, connu sous le nom de Congrès de Karlsruhe
Une époque de grands bouleversements – Meyer et Mendeleïev partagent plus qu’une quête commune. Les deux partageaient en fait le même professeur – Robert Busen, lui-même célèbre – à l’Université de Heidelberg à seulement cinq ans d’intervalle. En 1860, les deux jeunes scientifiques ont tous deux assisté au tout premier rassemblement international de chimistes, connu sous le nom de Congrès de Karlsruhe
À Karlsruhe, Meyer a été initié au concept de mesure des poids atomiques . Les années 1850 et 1860 ont été des décennies de découvertes scientifiques vastes et passionnantes : juste un an avant Karlsruhe, Charles Darwin avait publié son ouvrage fondateur De l’origine des espèces , brisant les vieux concepts avec l’idée d’évolution. L’année suivante, Bunsen contribuera à faire des percées dans le domaine de l’analyse spectrale.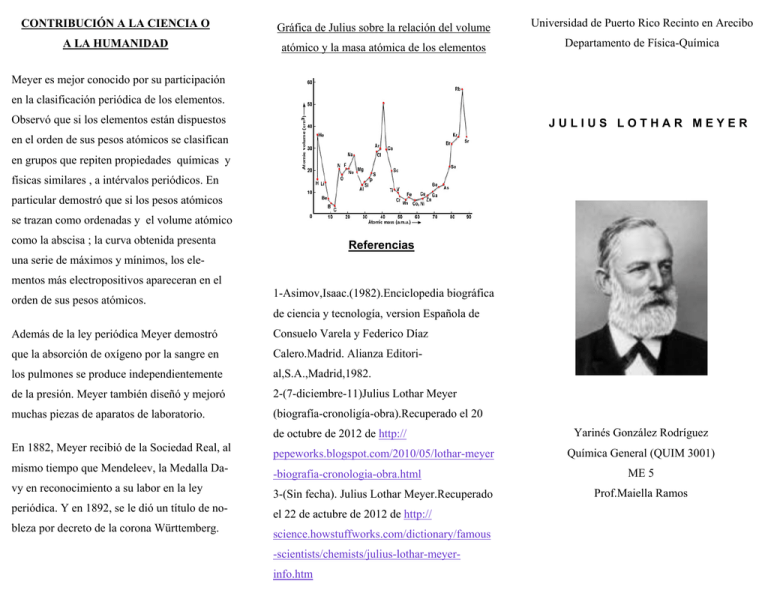 Au fur et à mesure des découvertes, un besoin s’est fait sentir d’aider à les organiser. C’est là que Meyer entre en jeu.
Au fur et à mesure des découvertes, un besoin s’est fait sentir d’aider à les organiser. C’est là que Meyer entre en jeu.
La grande percée – Meyer a passé cette période en tant qu’éducateur, travaillant à l’Université de Tübingen dans le sud de l’Allemagne. En 1864, il publie son propre manuel, Die modernen Theorien der Chemie , ou Modern Chemical Theory , qu’il dédie à Bunsen. Ici, Meyer a élaboré des idées dont la science et l’industrie avaient envie : comment cartographier et identifier les propriétés des éléments, dans l’espoir de les comprendre et de créer de nouveaux mélanges.
La théorie chimique moderne a mis un accent particulier sur la valence ou le pouvoir de combinaison. Valence examine de nombreux atomes d’hydrogène qui peuvent se former avec n’importe quel élément donné. Le composé ammoniac en est un bon exemple – composé d’azote et d’hydrogène, avec trois atomes d’azote et un hydrogène singulier, l’azote a une valence de trois. Meyer a démontré que, à mesure que la valence intégrale change, le poids atomique des éléments augmente. Le moment de Mendeleïev — En Russie, Mendeleïev était sur une voie similaire. Travaillant sur un manuel de chimie qui serait finalement publié en 1871, Mendeleev a publié les premiers articles relatifs aux tableaux périodiques en 1869.
Le moment de Mendeleïev — En Russie, Mendeleïev était sur une voie similaire. Travaillant sur un manuel de chimie qui serait finalement publié en 1871, Mendeleev a publié les premiers articles relatifs aux tableaux périodiques en 1869.
Le travail de Mendeleïev présentait des différences substantielles par rapport à celui de Meyer, dont certaines influenceraient la renommée future. Le travail de Mendeleev ne s’est pas contenté d’organiser tous les éléments connus du monde – il en a également prédit certains, une position que Meyer n’était pas disposé à adopter. Au fil des décennies et des siècles, les prédictions de Mendeleev se sont avérées exactes, faisant croître sa légende. En 1870, Meyer publie son propre tableau. Bien qu’il manque de prédictions, il a montré la même ampleur du travail de Mendeleev – et a été publié un an avant celui de Mendeleev. Meyer a pu apporter des contributions de fond de manière unique, avec des démonstrations graphiques de la relation entre le volume atomique et le poids atomique.
En 1870, Meyer publie son propre tableau. Bien qu’il manque de prédictions, il a montré la même ampleur du travail de Mendeleev – et a été publié un an avant celui de Mendeleev. Meyer a pu apporter des contributions de fond de manière unique, avec des démonstrations graphiques de la relation entre le volume atomique et le poids atomique. Une vie de réalisations régulières – Il semble qu’il n’y ait pas eu de rivalité sérieuse entre les deux hommes : satisfait de ses propres contributions et de son travail de professeur, Meyer n’a jamais défié Mendeleïev ou ses partisans pour savoir qui était le « premier » à l’idée d’une publication périodique. tableau. Il passera les vingt dernières années de sa vie à Tübingen une figure respectée dans le monde de la chimie, bien qu’un peu anonyme ailleurs.
Une vie de réalisations régulières – Il semble qu’il n’y ait pas eu de rivalité sérieuse entre les deux hommes : satisfait de ses propres contributions et de son travail de professeur, Meyer n’a jamais défié Mendeleïev ou ses partisans pour savoir qui était le « premier » à l’idée d’une publication périodique. tableau. Il passera les vingt dernières années de sa vie à Tübingen une figure respectée dans le monde de la chimie, bien qu’un peu anonyme ailleurs.
Julius Lothar Meyer (1830-1895) (Julius) Lothar Meyer était un chimiste allemand qui a découvert la loi périodique, indépendamment de Dmitry Mendeleïev, à peu près au même moment (1869). Cependant, il n’a pas développé la classification périodique des éléments chimiques aussi complètement que Mendeleïev. Meyer a été formé à l’origine en médecine et en chimie. Il a examiné l’effet du monoxyde de carbone sur le sang. En 1879, Meyer a comparé le volume atomique au poids atomique. Tracée sur un graphique, la courbe montre la périodicité des éléments. Il a également établi le concept de valence en indiquant qu’un élément donné se combinait avec un nombre caractéristique d’atomes d’hydrogène, et a inventé les termes comme univalent, bivalent et trivalent, basés sur ce nombre.
(Julius) Lothar Meyer était un chimiste allemand qui a découvert la loi périodique, indépendamment de Dmitry Mendeleïev, à peu près au même moment (1869). Cependant, il n’a pas développé la classification périodique des éléments chimiques aussi complètement que Mendeleïev. Meyer a été formé à l’origine en médecine et en chimie. Il a examiné l’effet du monoxyde de carbone sur le sang. En 1879, Meyer a comparé le volume atomique au poids atomique. Tracée sur un graphique, la courbe montre la périodicité des éléments. Il a également établi le concept de valence en indiquant qu’un élément donné se combinait avec un nombre caractéristique d’atomes d’hydrogène, et a inventé les termes comme univalent, bivalent et trivalent, basés sur ce nombre.
https://www.inverse.com/science/julius-lothar-meyer-google-doodle-august-19
https://www.scientificamerican.com/article/professor-lothar-meyer/

