 Comment la découverte de l’électron a bouleversé la perception du monde
Comment la découverte de l’électron a bouleversé la perception du monde C’est l’une des avancées les plus importantes de la physique moderne : la mise au jour de la première particule élémentaire.
C’est l’une des avancées les plus importantes de la physique moderne : la mise au jour de la première particule élémentaire.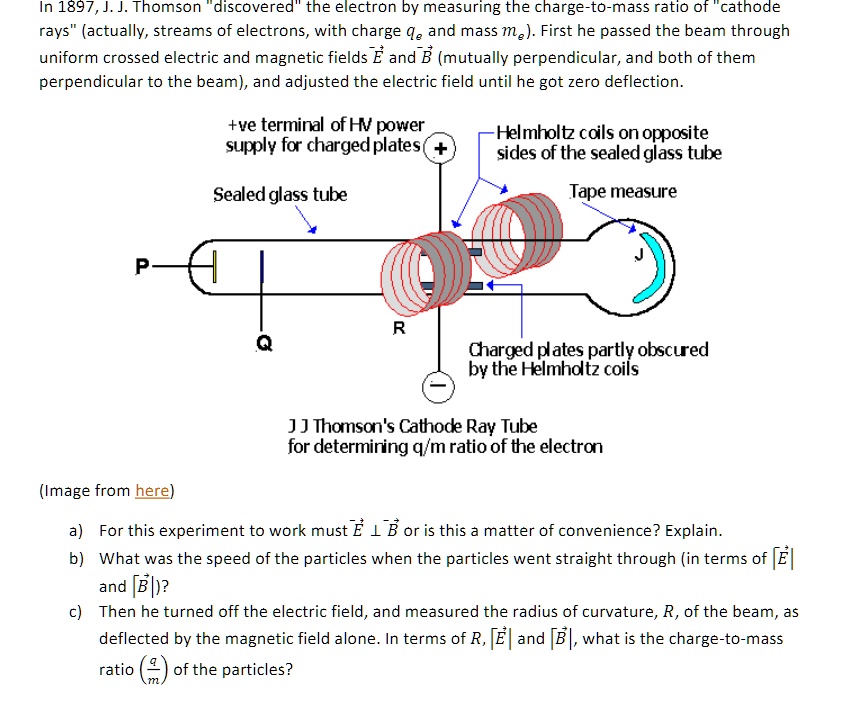 Le 30 avril 1897, le physicien britannique Joseph John Thomson (1856-1940) a annoncé sa découverte que les atomes étaient constitués de composants plus petits. Cette découverte a révolutionné la façon dont les scientifiques pensaient à l’atome et a eu des ramifications majeures pour le domaine de la physique. Bien que Thompson les ait appelés « corpuscules », ce qu’il a trouvé est plus communément connu aujourd’hui sous le nom d’électron.
Le 30 avril 1897, le physicien britannique Joseph John Thomson (1856-1940) a annoncé sa découverte que les atomes étaient constitués de composants plus petits. Cette découverte a révolutionné la façon dont les scientifiques pensaient à l’atome et a eu des ramifications majeures pour le domaine de la physique. Bien que Thompson les ait appelés « corpuscules », ce qu’il a trouvé est plus communément connu aujourd’hui sous le nom d’électron. L’humanité avait déjà découvert le courant électrique et l’avait exploité à bon escient, mais les scientifiques n’avaient pas encore observé la composition des atomes. Thomson, un professeur très respecté à Cambridge, a déterminé l’existence des électrons en étudiant les rayons cathodiques. Il a conclu que les particules composant les rayons étaient 1 000 fois plus légères que l’atome le plus léger, prouvant qu’il existait quelque chose de plus petit que les atomes. Thomson a comparé la composition des atomes au plume pudding, avec des « corpuscules » chargés négativement disséminés dans un champ chargé positivement.
L’humanité avait déjà découvert le courant électrique et l’avait exploité à bon escient, mais les scientifiques n’avaient pas encore observé la composition des atomes. Thomson, un professeur très respecté à Cambridge, a déterminé l’existence des électrons en étudiant les rayons cathodiques. Il a conclu que les particules composant les rayons étaient 1 000 fois plus légères que l’atome le plus léger, prouvant qu’il existait quelque chose de plus petit que les atomes. Thomson a comparé la composition des atomes au plume pudding, avec des « corpuscules » chargés négativement disséminés dans un champ chargé positivement. L’analogie du plume pudding a été réfutée par Ernest Rutherford, un étudiant et collaborateur de Thomson, dans le laboratoire de Thomson à Cambridge en 1910. La conclusion de Rutherford selon laquelle la charge positive d’un atome réside dans son noyau a établi le modèle de l’atome tel que nous le connaissons aujourd’hui.
L’analogie du plume pudding a été réfutée par Ernest Rutherford, un étudiant et collaborateur de Thomson, dans le laboratoire de Thomson à Cambridge en 1910. La conclusion de Rutherford selon laquelle la charge positive d’un atome réside dans son noyau a établi le modèle de l’atome tel que nous le connaissons aujourd’hui.  En plus de remporter son propre prix Nobel, Thomson a employé six assistants de recherche qui ont ensuite remporté des prix Nobel de physique et deux, dont Rutherford, qui a remporté des prix Nobel de chimie. Son fils, George Paget Thomson, a également remporté un prix Nobel pour son étude des électrons. Combiné à ses propres recherches, le réseau de chercheurs atomiques que Thomson a cultivé a donné à l’humanité une compréhension nouvelle et détaillée des plus petits éléments constitutifs de l’univers.
En plus de remporter son propre prix Nobel, Thomson a employé six assistants de recherche qui ont ensuite remporté des prix Nobel de physique et deux, dont Rutherford, qui a remporté des prix Nobel de chimie. Son fils, George Paget Thomson, a également remporté un prix Nobel pour son étude des électrons. Combiné à ses propres recherches, le réseau de chercheurs atomiques que Thomson a cultivé a donné à l’humanité une compréhension nouvelle et détaillée des plus petits éléments constitutifs de l’univers.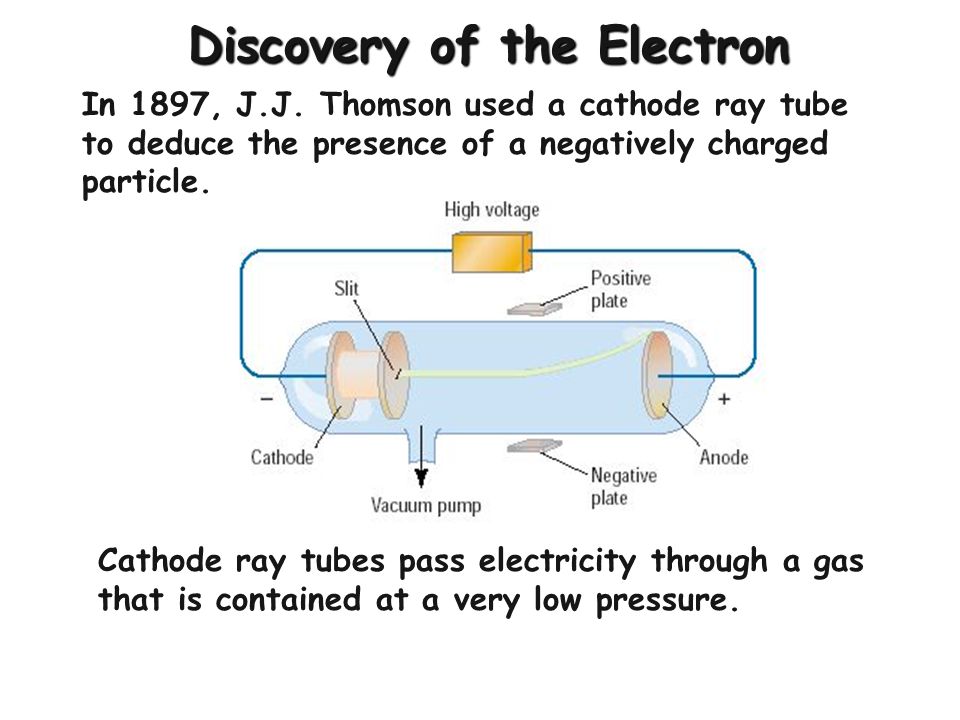 En 1897, le physicien JJ Thomson raconte à un auditoire scientifique surpris qu’il a découvert quelque chose de plus petit qu’un atome, une particule avec une masse minuscule et une charge négative. Certains dans le public de la Royal Institution of Great Britain ce vendredi soir ont dit plus tard à Thomson qu’ils pensaient qu’il « se tirait les jambes ». L’atome, après tout, était connu pour être indivisible. C’est ce que son nom signifiait.
En 1897, le physicien JJ Thomson raconte à un auditoire scientifique surpris qu’il a découvert quelque chose de plus petit qu’un atome, une particule avec une masse minuscule et une charge négative. Certains dans le public de la Royal Institution of Great Britain ce vendredi soir ont dit plus tard à Thomson qu’ils pensaient qu’il « se tirait les jambes ». L’atome, après tout, était connu pour être indivisible. C’est ce que son nom signifiait.
Les chercheurs avaient été intrigués par les rayons cathodiques jusqu’à ce que Thomson ait théorisé que les rayons étaient en fait des flux de petites particules subatomiques, les premières connues. Il les appelait « corpuscules », le latin pour « petits corps ». Thomson a estimé que ses corpuscules chargés négativement représentaient environ un millième de la masse d’un atome d’hydrogène (1/1836 ou 1/1837 est le rapport accepté aujourd’hui), correspondant à une charge positive ailleurs dans l’atome. Thomson était vague en 1897 mais a théorisé plus tard que les électrons négatifs pullulaient dans une « sphère d’électrification positive uniforme ». (Établir le modèle orbital nucléaire de l’atome reviendrait à Ernest Rutherford et Niels Bohr dans les décennies suivantes.)
Thomson a estimé que ses corpuscules chargés négativement représentaient environ un millième de la masse d’un atome d’hydrogène (1/1836 ou 1/1837 est le rapport accepté aujourd’hui), correspondant à une charge positive ailleurs dans l’atome. Thomson était vague en 1897 mais a théorisé plus tard que les électrons négatifs pullulaient dans une « sphère d’électrification positive uniforme ». (Établir le modèle orbital nucléaire de l’atome reviendrait à Ernest Rutherford et Niels Bohr dans les décennies suivantes.)
Dans un commentaire sur la version publiée de la conférence de Thomson, le physicien irlandais George F. FitzGerald a suggéré que les corpuscules étaient en fait des électrons libres. D’autres scientifiques avaient proposé que les rayons cathodiques étaient composés de particules et avaient tenté d’établir leur masse et leur charge relatives. La grande contribution de Thomson a été d’estimer ce ratio et de reconnaître que le ratio était universel et ne dépendait pas des matériaux spécifiques. Cela l’a amené à postuler que les particules étaient l’un des éléments constitutifs de l’atome lui-même, même s’il ne l’avait pas entièrement prouvé au moment de sa conférence d’époque.
D’autres scientifiques avaient proposé que les rayons cathodiques étaient composés de particules et avaient tenté d’établir leur masse et leur charge relatives. La grande contribution de Thomson a été d’estimer ce ratio et de reconnaître que le ratio était universel et ne dépendait pas des matériaux spécifiques. Cela l’a amené à postuler que les particules étaient l’un des éléments constitutifs de l’atome lui-même, même s’il ne l’avait pas entièrement prouvé au moment de sa conférence d’époque. Thomson a reçu le prix Nobel de 1906 « en reconnaissance des grands mérites de ses recherches théoriques et expérimentales sur la conduction de l’électricité par les gaz ». Il a été anobli en 1908.
Thomson a reçu le prix Nobel de 1906 « en reconnaissance des grands mérites de ses recherches théoriques et expérimentales sur la conduction de l’électricité par les gaz ». Il a été anobli en 1908.
Son livre de 1907 s’intitulait The Corpuscular Theory of Matter, et il a continué à appeler sa découverte « corpuscules » jusqu’en 1913. Les électrons sont des sphères presque parfaites
Les électrons sont des sphères presque parfaites
Pour être précis, l’électron diffère d’être parfaitement rond de moins de 0,000000000000000000000000001 cm. Pour mettre cela en contexte ; si un électron était de la taille du système solaire, il ne serait pas parfaitement rond de moins de la largeur d’un cheveu humain.) L’équipe de l’Imperial College à l’origine de la recherche, qui a été menée sur des molécules de fluorure d’ytterbium, a utilisé un laser pour mesurer le mouvement des électrons, et en particulier l’oscillation qu’ils présentent lorsqu’ils tournent. Ils n’ont observé aucune oscillation de ce type, ce qui implique que l’électron est parfaitement rond aux niveaux de précision disponibles, reflétés dans la figure ci-dessus.
L’équipe de l’Imperial College à l’origine de la recherche, qui a été menée sur des molécules de fluorure d’ytterbium, a utilisé un laser pour mesurer le mouvement des électrons, et en particulier l’oscillation qu’ils présentent lorsqu’ils tournent. Ils n’ont observé aucune oscillation de ce type, ce qui implique que l’électron est parfaitement rond aux niveaux de précision disponibles, reflétés dans la figure ci-dessus. Le co-auteur du rapport décrivant la recherche, Jony Hudson, a déclaré : « Nous sommes vraiment ravis d’avoir pu améliorer nos connaissances sur l’un des éléments de base de la matière. Cela a été une mesure très difficile à faire. , mais cette connaissance nous permettra d’améliorer nos théories de la physique fondamentale. Les gens sont souvent surpris d’entendre que nos théories de la physique ne sont pas « terminées », mais en vérité elles sont constamment affinées et améliorées en faisant des mesures toujours plus précises comme celle-ci.»
Le co-auteur du rapport décrivant la recherche, Jony Hudson, a déclaré : « Nous sommes vraiment ravis d’avoir pu améliorer nos connaissances sur l’un des éléments de base de la matière. Cela a été une mesure très difficile à faire. , mais cette connaissance nous permettra d’améliorer nos théories de la physique fondamentale. Les gens sont souvent surpris d’entendre que nos théories de la physique ne sont pas « terminées », mais en vérité elles sont constamment affinées et améliorées en faisant des mesures toujours plus précises comme celle-ci.» La prochaine étape consiste à augmenter encore ce niveau de précision, en utilisant de nouvelles méthodes pour refroidir les molécules à des températures extrêmement basses et contrôler leur mouvement. Les résultats sont importants pour l’étude de l’antimatière, et en particulier du positon, qui devrait se comporter de manière identique à l’électron mais avec une charge électrique opposée. Si plus de différences peuvent être trouvées, cela pourrait aider à expliquer pourquoi beaucoup moins d’antimatière a été découverte dans l’univers que prévu par la théorie.
La prochaine étape consiste à augmenter encore ce niveau de précision, en utilisant de nouvelles méthodes pour refroidir les molécules à des températures extrêmement basses et contrôler leur mouvement. Les résultats sont importants pour l’étude de l’antimatière, et en particulier du positon, qui devrait se comporter de manière identique à l’électron mais avec une charge électrique opposée. Si plus de différences peuvent être trouvées, cela pourrait aider à expliquer pourquoi beaucoup moins d’antimatière a été découverte dans l’univers que prévu par la théorie.
JJ Thomson, au complet Sir Joseph John Thomson, (né le 18 décembre 1856 à Cheetham Hill, près de Manchester, Angleterre—mort le 30 août 1940 à Cambridge, Cambridgeshire), physicien anglais qui a contribué à révolutionner la connaissance de la structure atomique par sa découverte de l’électron (1897). Il a reçu le prix Nobel de physique en 1906 et a été anobli en 1908. Le siècle de l’électron
Le siècle de l’électron Centenaire survenue le 30 avril 1897, au terme de plusieurs siècles d’avancées successives des savants sur la nature des phénomènes électriques, la découverte de l’électron par le Britannique Joseph John Thomson a ouvert la voie à la physique atomique. Notre représentation de la structure intime de la matière et de l’Univers a été totalement bouleversée par les recherches menées depuis un siècle dans cette discipline. Les modèles théoriques élaborés par les chercheurs pour décrire le comportement des constituants de l’atome ne parviennent pas encore à expliquer certaines caractéristiques des particules élémentaires qui le composent et, notamment, l’origine de leur masse.
Centenaire survenue le 30 avril 1897, au terme de plusieurs siècles d’avancées successives des savants sur la nature des phénomènes électriques, la découverte de l’électron par le Britannique Joseph John Thomson a ouvert la voie à la physique atomique. Notre représentation de la structure intime de la matière et de l’Univers a été totalement bouleversée par les recherches menées depuis un siècle dans cette discipline. Les modèles théoriques élaborés par les chercheurs pour décrire le comportement des constituants de l’atome ne parviennent pas encore à expliquer certaines caractéristiques des particules élémentaires qui le composent et, notamment, l’origine de leur masse. 
 Certains diront que c’est l’ère spatiale. Aucune de ces réponses n’est fausse, bien qu’aucune d’entre elles ne puisse décrire la révolution scientifique du vingtième siècle dans sa totalité. Si l’on regarde en arrière, on constate que la prolifération des connaissances scientifiques que l’on perçoit au XXe siècle trouve son origine dans un déclencheur donné par un événement unique, à savoir la découverte de l’électron mature, de sorte que l’ancienne physique a dû céder la place à une nouvelle.
Certains diront que c’est l’ère spatiale. Aucune de ces réponses n’est fausse, bien qu’aucune d’entre elles ne puisse décrire la révolution scientifique du vingtième siècle dans sa totalité. Si l’on regarde en arrière, on constate que la prolifération des connaissances scientifiques que l’on perçoit au XXe siècle trouve son origine dans un déclencheur donné par un événement unique, à savoir la découverte de l’électron mature, de sorte que l’ancienne physique a dû céder la place à une nouvelle.  D’une certaine manière, le XXe siècle a été le siècle de l’électron. Cette refonte, cependant, n’a pas rendu l’ancienne science fausse, mais a établi les nouvelles limites de son applicabilité et est devenue le cas particulier d’une connaissance plus généralisée que la révolution du XXe siècle a rejetée.
D’une certaine manière, le XXe siècle a été le siècle de l’électron. Cette refonte, cependant, n’a pas rendu l’ancienne science fausse, mais a établi les nouvelles limites de son applicabilité et est devenue le cas particulier d’une connaissance plus généralisée que la révolution du XXe siècle a rejetée.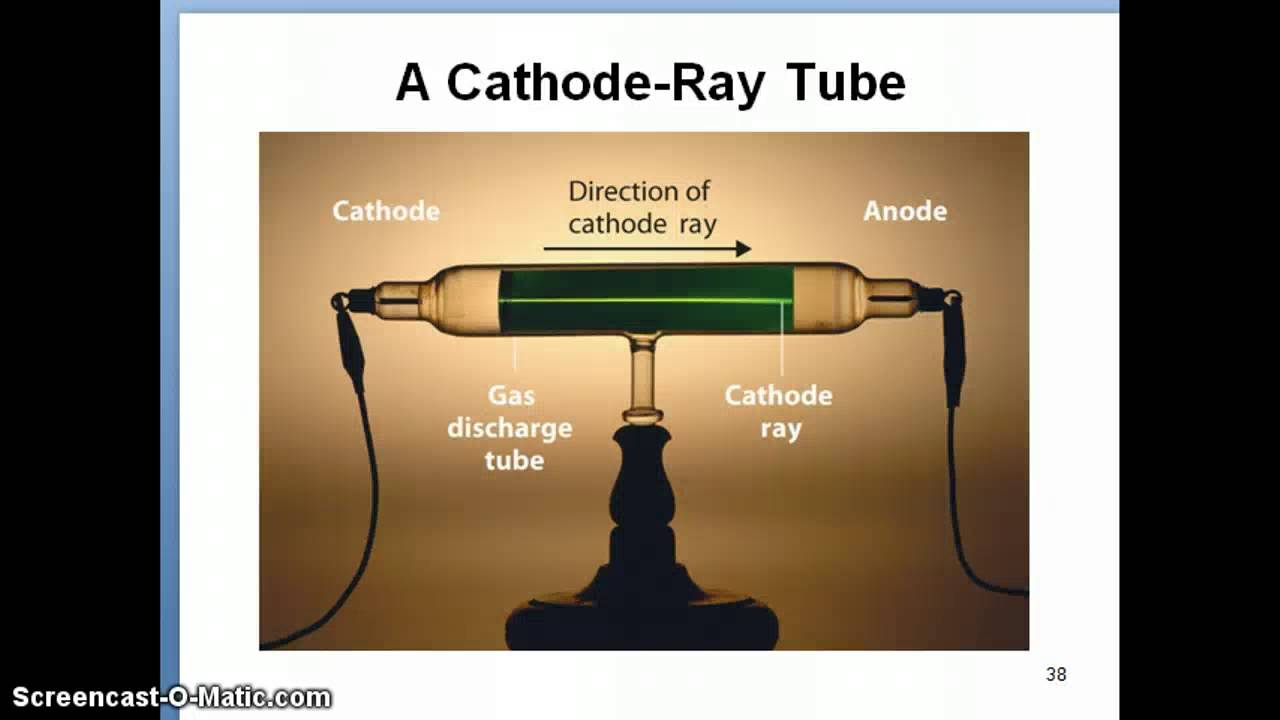 La découverte :
La découverte :
La découverte de l’électron, en fait, a été un choc pour beaucoup. C’est parce que, même dans les années 1890, la théorie atomique de la matière n’avait pas été unanimement acceptée par la communauté des physiciens. Dire à cette époque que même l’atome est divisible relevait d’une audacieuse initiative de la part du découvreur. Les opposants à l’atomisme étaient un groupe de philosophes qui se disaient machistes, c’est-à-dire les disciples du mathématicien-physicien allemand Ernst Mach. Ils ont émis l’hypothèse que le monde doit être représenté en termes de sensations. Les sensations ne permettant pas de « sentir » un atome, ils rejettent l’atomisme, qui les conduit à leur tour au rejet du matérialisme (si l’oppression ne se fait pas sentir, cesse-t-elle d’exister ?). La bataille de Lénine contre les machistes établis et certains soi-disant marxistes (mais machistes voilés) nécessite un essai différent. Mais la défaite du machisme est survenue dans le domaine de la science elle-même, que nous décrivons ci-dessous.
 Ces « quelques chose » pourraient être déviées électromagnétiquement. Par ces déviations électromagnétiques, Thomson a essayé de trouver le rapport entre la charge (e) et la masse (m) de ces « quelque chose » dans les rayons cathodiques. Il a découvert que les particules étaient chargées négativement et que la valeur (e/m) était la même quel que soit le gaz avec lequel il remplissait le tube à rayons cathodiques et dans tous les cas, la valeur était 1840 fois supérieure à ce qu’il avait prévu pour l’hydrogène. Il est arrivé à une conclusion audacieuse : cet objet doit être présent dans tous les atomes et est chargé négativement. De plus, il doit être subatomique puisqu’une valeur aussi élevée (e/m) ne peut venir que si m est extrêmement petit c’est-à-dire si sa masse est (1/1840) de la masse de l’atome d’hydrogène. Cela signifiait que le plus petit atome, c’est-à-dire même celui de l’hydrogène devait contenir cette particule Atome est donc divisible.
Ces « quelques chose » pourraient être déviées électromagnétiquement. Par ces déviations électromagnétiques, Thomson a essayé de trouver le rapport entre la charge (e) et la masse (m) de ces « quelque chose » dans les rayons cathodiques. Il a découvert que les particules étaient chargées négativement et que la valeur (e/m) était la même quel que soit le gaz avec lequel il remplissait le tube à rayons cathodiques et dans tous les cas, la valeur était 1840 fois supérieure à ce qu’il avait prévu pour l’hydrogène. Il est arrivé à une conclusion audacieuse : cet objet doit être présent dans tous les atomes et est chargé négativement. De plus, il doit être subatomique puisqu’une valeur aussi élevée (e/m) ne peut venir que si m est extrêmement petit c’est-à-dire si sa masse est (1/1840) de la masse de l’atome d’hydrogène. Cela signifiait que le plus petit atome, c’est-à-dire même celui de l’hydrogène devait contenir cette particule Atome est donc divisible. La première prédiction de l’électron a cependant été faite par Stoney, qui avait théoriquement calculé la charge de l’électron, en utilisant les lois de l’électrolyse de Faraday. Comme décrit ci-dessus, le chemin de la découverte a emprunté une voie entièrement différente et était impossible sans les machines et les instruments que la révolution industrielle en Angleterre avait mis au point. Une mention de ce fait devrait être faite, afin de répondre tête baissée aux revivalistes (la brigade du safran en particulier) qui prétendent souvent que tout ce que la science moderne a donné à l’homme était connu de nos anciens ancêtres. Dans un souci d’objectivité, il convient d’avancer que les découvertes d’un certain type sont vraiment caractéristiques de l’époque. La découverte de l’électron dans la phase de révolution préindustrielle est une absurdité. Il est vrai que les découvertes scientifiques arrivent souvent par hasard. Mais ces accidents aussi ne sont perçus que par des esprits scientifiques mûrs par rapport aux connaissances scientifiques connues à cette époque. De même, la découverte de l’électron ou de la radioactivité qui a suivi, ne peut apparaître qu’à 19laboratoires scientifiques du XXe siècle et impossible dans les séminaires d’advaitavada ou de mayavada, comme cela est illustré ci-dessous dans le contexte du machisme.
La première prédiction de l’électron a cependant été faite par Stoney, qui avait théoriquement calculé la charge de l’électron, en utilisant les lois de l’électrolyse de Faraday. Comme décrit ci-dessus, le chemin de la découverte a emprunté une voie entièrement différente et était impossible sans les machines et les instruments que la révolution industrielle en Angleterre avait mis au point. Une mention de ce fait devrait être faite, afin de répondre tête baissée aux revivalistes (la brigade du safran en particulier) qui prétendent souvent que tout ce que la science moderne a donné à l’homme était connu de nos anciens ancêtres. Dans un souci d’objectivité, il convient d’avancer que les découvertes d’un certain type sont vraiment caractéristiques de l’époque. La découverte de l’électron dans la phase de révolution préindustrielle est une absurdité. Il est vrai que les découvertes scientifiques arrivent souvent par hasard. Mais ces accidents aussi ne sont perçus que par des esprits scientifiques mûrs par rapport aux connaissances scientifiques connues à cette époque. De même, la découverte de l’électron ou de la radioactivité qui a suivi, ne peut apparaître qu’à 19laboratoires scientifiques du XXe siècle et impossible dans les séminaires d’advaitavada ou de mayavada, comme cela est illustré ci-dessous dans le contexte du machisme. La découverte de l’électron fut tout aussi choquante pour les Machistes car il y avait là quelque chose qui, à leur sens, ne permettait pas de le percevoir et pourtant c’était là ! Et que ce n’était pas la « manifestation de l’éther » (un objet mystique) comme les Machistes avaient décrit les rayons cathodiques, mais la VRAIE MATIÈRE. Il a en outre prouvé que la matière non plus ne s’épuise pas avec l’atome mais peut exister en tant que particules « subatomiques » comme l’a montré l’existence de l’électron. Cette inépuisabilité de la matière établie par la découverte des électrons fut un coup écrasant dont Machist ne se remit jamais.
La découverte de l’électron fut tout aussi choquante pour les Machistes car il y avait là quelque chose qui, à leur sens, ne permettait pas de le percevoir et pourtant c’était là ! Et que ce n’était pas la « manifestation de l’éther » (un objet mystique) comme les Machistes avaient décrit les rayons cathodiques, mais la VRAIE MATIÈRE. Il a en outre prouvé que la matière non plus ne s’épuise pas avec l’atome mais peut exister en tant que particules « subatomiques » comme l’a montré l’existence de l’électron. Cette inépuisabilité de la matière établie par la découverte des électrons fut un coup écrasant dont Machist ne se remit jamais. Mais c’était en fait l’influence de Mach qui avait retardé la découverte de l’électron. Les rayons X qui ont été découverts par Röntgen en 1895, nous le savons, sont causés par des processus électroniques. En 1896, Alfred Zeeman découvre l’effet Zeeman. Son explication, telle que nous la connaissons aujourd’hui, est basée sur le mouvement des électrons à l’intérieur de l’atome lorsqu’un champ magnétique a été appliqué. Mais ces scientifiques ne pouvaient pas s’avancer et déclarer la découverte de l’électron, comme l’a fait Thomson, compte tenu de deux facteurs. Premièrement, leur témoignage était indirect. Deuxièmement, l’influence de Mach en Europe étant trop forte, ils réfléchissaient, hésitaient et même doutaient de ce qu’ils savaient. L’Angleterre était relativement à l’abri de l’influence des Machistes et, par conséquent, l’audace de Thomson avait moins d’obstacles. La découverte de l’électron a été la dernière grande découverte scientifique du XIXe siècle. Avec l’arrivée de l’électron, la science du vingtième siècle est vraiment arrivée et à chaque année qui a suivi, l’ancien monde de la physique s’est effondré.
Mais c’était en fait l’influence de Mach qui avait retardé la découverte de l’électron. Les rayons X qui ont été découverts par Röntgen en 1895, nous le savons, sont causés par des processus électroniques. En 1896, Alfred Zeeman découvre l’effet Zeeman. Son explication, telle que nous la connaissons aujourd’hui, est basée sur le mouvement des électrons à l’intérieur de l’atome lorsqu’un champ magnétique a été appliqué. Mais ces scientifiques ne pouvaient pas s’avancer et déclarer la découverte de l’électron, comme l’a fait Thomson, compte tenu de deux facteurs. Premièrement, leur témoignage était indirect. Deuxièmement, l’influence de Mach en Europe étant trop forte, ils réfléchissaient, hésitaient et même doutaient de ce qu’ils savaient. L’Angleterre était relativement à l’abri de l’influence des Machistes et, par conséquent, l’audace de Thomson avait moins d’obstacles. La découverte de l’électron a été la dernière grande découverte scientifique du XIXe siècle. Avec l’arrivée de l’électron, la science du vingtième siècle est vraiment arrivée et à chaque année qui a suivi, l’ancien monde de la physique s’est effondré.
C’est la résolution de cette crise qui a conduit à la révolution en ouvrant des percées conceptuelles dans deux directions différentes à savoir par la découverte de (a) la théorie de la relativité et (b) la mécanique quantique. Ce n’est pas le but de cet essai de traiter des prises de position philosophiques de ces idées révolutionnaires vis-à-vis de notre conceptualisation de la nature. Les progrès scientifiques qui ont suivi n’ont pas non plus été unidirectionnels. Cette idée peut être mieux exprimée par un organigramme, même si cela semble assez formidable. Je n’ai pas eu l’idée de dresser une liste exhaustive des développements scientifiques qui ont eu lieu au XXe siècle. Pour décrire les événements, le mieux serait d’utiliser un film avec des flashbacks, des flashbacks intérieurs ou de les mettre sur un CD et d’aller et venir par différents chemins en cliquant avec la souris. Ce bref récit montrera comment la prolifération et la diversification dans différents domaines ont eu lieu en même temps, les domaines émergents se sont également renforcés les uns les autres. Ici aussi, nous ne choisissons que quelques exemples sélectionnés. Le voyage ici bien qu’unidimensionnel ne l’est pas réellement.
C’est la contrainte de l’espace qui nous limite à une telle narration et nous espérons que des articles sur des sujets similaires seront publiés à l’avenir par d’autres auteurs également.
C’est la contrainte de l’espace qui nous limite à une telle narration et nous espérons que des articles sur des sujets similaires seront publiés à l’avenir par d’autres auteurs également. . C’est la contrainte de l’espace qui nous limite à une telle narration et nous espérons que des articles sur des sujets similaires seront publiés à l’avenir par d’autres auteurs également.
En 1897, lors du discours du vendredi soir de la Royal Institution, J.J. Thomson a annoncé pour la première fois l’existence des électrons (comme on les appelle aujourd’hui). Thomson a expliqué à son auditoire que, plus tôt dans l’année, il avait fait une découverte surprenante. Il avait trouvé une particule de matière mille fois plus petite que l’atome. Il l’appelle un corpuscule, ce qui signifie « petit corps ». Bien que Thomson soit le directeur du laboratoire Cavendish de l’université de Cambridge et l’un des scientifiques les plus respectés de Grande-Bretagne, les scientifiques présents ont eu du mal à croire la nouvelle. Ils pensaient que l’atome était la partie la plus petite et indivisible de la matière qui pouvait exister. Néanmoins, l’électron est la première particule élémentaire à être découverte.
Électron En 1897, lors du discours du vendredi soir de la Royal Institution, Joseph John Thomson (1856-1940) annonça pour la première fois l’existence des électrons (ainsi qu’ils sont maintenant nommés). Thomson a déclaré à son auditoire qu’au début de l’année, il avait fait une découverte surprenante. Il avait trouvé une particule de matière mille fois plus petite que l’atome. Il l’a appelé un corpuscule, ce qui signifie «petit corps». Bien que Thomson ait été directeur du laboratoire Cavendish de l’Université de Cambridge et l’un des scientifiques les plus respectés de Grande-Bretagne, les scientifiques présents ont trouvé la nouvelle difficile à croire. Ils pensaient que l’atome était la partie la plus petite et indivisible de la matière qui pouvait exister. Néanmoins, l’électron a été la première particule élémentaire à être découverte.
En 1897, lors du discours du vendredi soir de la Royal Institution, Joseph John Thomson (1856-1940) annonça pour la première fois l’existence des électrons (ainsi qu’ils sont maintenant nommés). Thomson a déclaré à son auditoire qu’au début de l’année, il avait fait une découverte surprenante. Il avait trouvé une particule de matière mille fois plus petite que l’atome. Il l’a appelé un corpuscule, ce qui signifie «petit corps». Bien que Thomson ait été directeur du laboratoire Cavendish de l’Université de Cambridge et l’un des scientifiques les plus respectés de Grande-Bretagne, les scientifiques présents ont trouvé la nouvelle difficile à croire. Ils pensaient que l’atome était la partie la plus petite et indivisible de la matière qui pouvait exister. Néanmoins, l’électron a été la première particule élémentaire à être découverte. J.J. Thomson (1856-1940)
J.J. Thomson (1856-1940)
https://www.history.com/this-day-in-history/jj-thomson-announces-discovery-of-electrons
https://www.wired.com/2012/04/april-30-1897-j-j-thomson-announces-the-electron-sort-of/
https://web.lemoyne.edu/~giunta/ea/THOMSONann.HTML
https://www-wired-com./2011/05/electrons-are-near-perfect-spheres/
https://www.cpim.org/marxist/200304_marxist_electron.htm