


Daniel Rutherford – découvreur de l’azote gazeux 
Rutherford était célèbre pour sa découverte de l’azote gazeux et des thermomètres à maximum et minimum. La méthode suivante est utilisée par Rutherford pour isoler l’azote 


L’azote gazeux est un gaz industriel produit par la distillation fractionnée d’air liquide, ou par des moyens mécaniques utilisant de l’air gazeux. L’azote commercial est souvent un sous-produit du traitement de l’air pour une concentration industrielle d’oxygène pour la fabrication de l’acier et à d’autres fins.
NH 4 Cl (aq) + NaNO2 (aq) → N 2(g) + NaCl (aq) + 2 H 2 O(l)
Faits sur l’azote L’azote est un gaz incolore, inodore et insipide qui est l’élément le plus abondant de l’atmosphère terrestre et est un constituant de toute matière vivante et il appartient à l’élément non métallique du groupe 15 du tableau périodique. C’est le pnictogène le plus léger et à température ambiante, c’est un gaz diatomique incolore et inodore. L’azote est un élément commun dans l’univers, estimé à environ le septième en abondance totale dans notre galaxie et le système solaire. L’azote est un non-métal, avec une électronégativité de 3,04. Il a cinq électrons dans sa coque externe et est donc trivalent dans la plupart des composés. Azote utilisé sous forme d’atmosphère modifiée, pur ou mélangé à du dioxyde de carbone, pour azote et préserver la fraîcheur des aliments emballés ou en vrac (en retardant le rancissement et d’autres formes de dommages oxydatifs).
L’azote est un gaz incolore, inodore et insipide qui est l’élément le plus abondant de l’atmosphère terrestre et est un constituant de toute matière vivante et il appartient à l’élément non métallique du groupe 15 du tableau périodique. C’est le pnictogène le plus léger et à température ambiante, c’est un gaz diatomique incolore et inodore. L’azote est un élément commun dans l’univers, estimé à environ le septième en abondance totale dans notre galaxie et le système solaire. L’azote est un non-métal, avec une électronégativité de 3,04. Il a cinq électrons dans sa coque externe et est donc trivalent dans la plupart des composés. Azote utilisé sous forme d’atmosphère modifiée, pur ou mélangé à du dioxyde de carbone, pour azote et préserver la fraîcheur des aliments emballés ou en vrac (en retardant le rancissement et d’autres formes de dommages oxydatifs).
L’azote est couramment utilisé lors des procédures de préparation d’échantillons pour l’analyse chimique. Il est utilisé pour concentrer et réduire le volume des échantillons liquides. L’azote peut être utilisé en remplacement ou en combinaison avec le dioxyde de carbone pour pressuriser les fûts de certaines bières. Les réservoirs d’azote remplacent également le dioxyde de carbone comme principale source d’alimentation des pistolets de paintball. L’azote doit être maintenu à une pression plus élevée que le CO2, ce qui rend les réservoirs de N2 plus lourds et plus chers. Il est utilisé dans les pièges à froid de certains équipements de laboratoire et pour refroidir les détecteurs infrarouges ou les détecteurs de rayons X. Il a également été utilisé pour refroidir les unités centrales de traitement et d’autres appareils dans les ordinateurs qui sont overclockés et qui produisent plus de chaleur que pendant le fonctionnement normal.
Isolement de l’azote 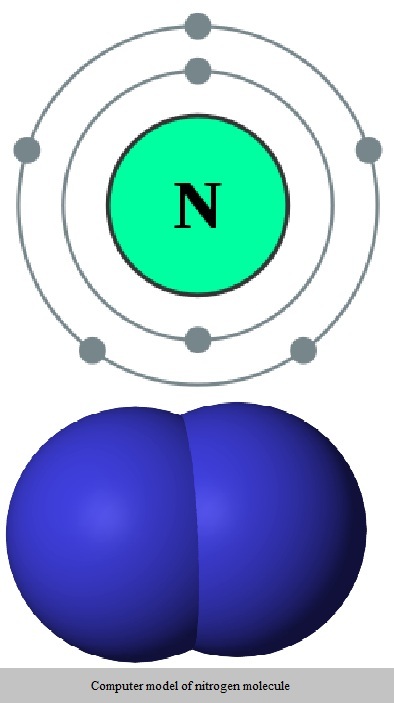
Lorsque Joseph Black étudiait les propriétés du dioxyde de carbone, il découvrit qu’une bougie ne pouvait pas y brûler. Lorsqu’une bougie était brûlée dans un récipient d’air fermé, la bougie finirait par s’éteindre et l’air restant ne supporterait pas de flamme. C’était normal, mais lorsque le dioxyde de carbone (causé par la bougie) était absorbé par des produits chimiques, une partie de l’air n’était pas absorbée. L’air qui restait ne supportait pas de flamme. Il confia ce problème à son élève de l’époque, Daniel Rutherford. Rutherford a gardé une souris dans un espace avec une qualité d’air confinée jusqu’à ce qu’elle meure. Ensuite, il brûla une bougie dans l’air restant jusqu’à ce qu’elle s’éteigne. Ensuite, il y brûla du phosphore jusqu’à ce qu’il ne brûle plus. Ensuite, l’air a été passé à travers une solution absorbant le dioxyde de carbone. L’air restant ne supportait pas la combustion et une souris ne pouvait pas y vivre. Rutherford a appelé le gaz (dont nous savons maintenant qu’il se composait principalement d’azote) « air nocif » ou « air phlogistiqué ».
Rutherford a rapporté l’expérience en 1772. Lui et Black étaient convaincus de la validité de la théorie du phlogistique, ils ont donc expliqué leurs résultats en termes de théorie. Ils ont dit que lorsque les souris respiraient et que la combustion se créait, du phlogistique se dégageait et pénétrait dans l’air, avec le dioxyde de carbone. Lorsque le dioxyde de carbone a ensuite été absorbé, l’air contenait encore du phlogistique. En fait, l’air en était saturé. C’est pourquoi les bougies et autres objets n’y brûlaient pas. Rutherford croyait que, de la même manière, une créature vivante abandonne le phlogistique en respirant et lorsqu’elle est placée dans de l’air déjà saturé de phlogistique, ne peut plus respirer et doit mourir.
Daniel Rutherford (1749-1819)
Chimiste et photographe écossais qui a découvert la partie de l’air qui ne supporte pas la combustion, maintenant connue sous le nom d’azote. Après avoir laissé une souris vivre dans une quantité confinée d’air jusqu’à ce qu’elle meure, il brûla une bougie et brûla du phosphore dans le même air aussi longtemps qu’ils brûleraient. Il a supposé que le gaz restant était du dioxyde de carbone, qu’il a dissous en le faisant passer à travers un alcali fort. Pourtant, il restait du gaz incapable d’entretenir la respiration ou la combustion dont il savait qu’il ne contenait plus d’oxygène ni de gaz carbonique. Il l’a appelé «l’air phlogistiqué», suivant la théorie du phlogistique de Georg Stahl. Il a ensuite été correctement décrit par Antoine Lavoisier. Rutherford a également conçu le premier thermomètre à maximum et minimum. En 1772, il décrit sa propre découverte de l’air «nocif» ou «phlogistiqué», maintenant connu sous le nom d’azote. Daniel Rutherford et ses deux sœurs sont tombés malades le même jour et sont décédés à une semaine d’intervalle.
https://www.nrscotland.gov.uk/research/learning/hall-of-fame/hall-of-fame-a-z/rutherford-daniel
https://www.chemeurope.com/en/encyclopedia/Daniel_Rutherford.html
