 Des scientifiques australiens implantent le premier prototype d’un «œil bionique» à un patient
Des scientifiques australiens implantent le premier prototype d’un «œil bionique» à un patient  Vision bionique
Vision bionique Œil bionique — mythes et réalité
Œil bionique — mythes et réalité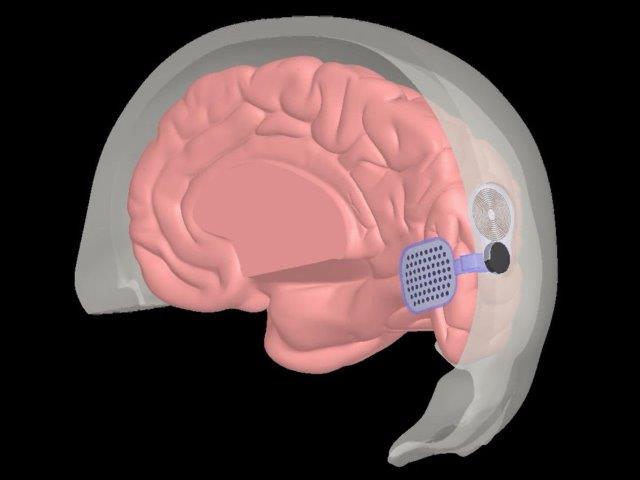 Des scientifiques de l’Université de Stanford développent un prototype d’œil bionique
Des scientifiques de l’Université de Stanford développent un prototype d’œil bionique
 Une équipe de scientifiques australiens a implanté un premier prototype d' »œil bionique » chez un patient qui a subi une perte de vision profonde due à une rétinite pigmentaire , une maladie génétique. Un communiqué de l’Université de Melbourne décrit la prothèse rétinienne, qui consiste en un implant rétinien avec 24 électrodes.
Une équipe de scientifiques australiens a implanté un premier prototype d' »œil bionique » chez un patient qui a subi une perte de vision profonde due à une rétinite pigmentaire , une maladie génétique. Un communiqué de l’Université de Melbourne décrit la prothèse rétinienne, qui consiste en un implant rétinien avec 24 électrodes.
Dans cette vidéo récemment publiée , les chercheurs discutent du processus de conception, de construction et de test de ce premier prototype pour garantir sa sécurité et son efficacité pour l’implantation humaine. De plus, la récipiendaire partage son expérience de participation au projet.
De même, des chercheurs de Stanford ont développé une prothèse rétinienne qui utilise la lumière proche infrarouge pour fournir des images et continuent de tester et d’affiner le dispositif.
La prothèse rétinienne développée par Stanford utilise une lumière proche infrarouge pour transmettre des images Une équipe de scientifiques australiens a implanté un premier prototype d' »œil bionique » chez un patient qui a subi une perte de vision profonde due à une rétinite pigmentaire , une maladie génétique. Un communiqué de l’Université de Melbourne décrit la prothèse rétinienne, qui consiste en un implant rétinien avec 24 électrodes.
Une équipe de scientifiques australiens a implanté un premier prototype d' »œil bionique » chez un patient qui a subi une perte de vision profonde due à une rétinite pigmentaire , une maladie génétique. Un communiqué de l’Université de Melbourne décrit la prothèse rétinienne, qui consiste en un implant rétinien avec 24 électrodes.
Dans cette vidéo récemment publiée , les chercheurs discutent du processus de conception, de construction et de test de ce premier prototype pour garantir sa sécurité et son efficacité pour l’implantation humaine. De plus, la récipiendaire partage son expérience de participation au projet.
De même, des chercheurs de Stanford ont développé une prothèse rétinienne qui utilise la lumière proche infrarouge pour fournir des images et continuent de tester et d’affiner le dispositif.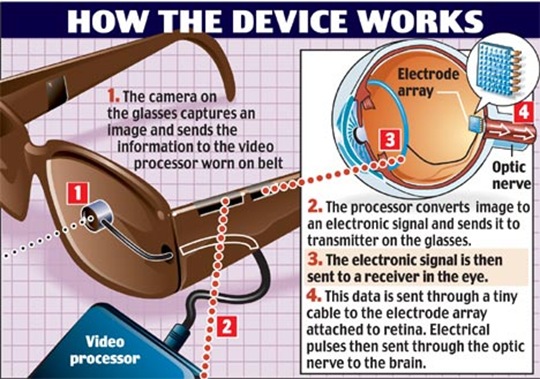 Les scientifiques ici ont développé une prothèse rétinienne innovante qui pourrait un jour rendre la vue à ceux qui ont perdu la vue en raison de certains types de maladies oculaires dégénératives.
Les scientifiques ici ont développé une prothèse rétinienne innovante qui pourrait un jour rendre la vue à ceux qui ont perdu la vue en raison de certains types de maladies oculaires dégénératives.
 Les courants électriques des photodiodes sur la puce déclencheraient alors des signaux dans la rétine, qui se dirigeraient ensuite vers le cerveau, permettant au patient de retrouver la vision.
Les courants électriques des photodiodes sur la puce déclencheraient alors des signaux dans la rétine, qui se dirigeraient ensuite vers le cerveau, permettant au patient de retrouver la vision.
Une étude , publiée en ligne le 13 mai dans Nature Photonics , montre comment les scientifiques ont utilisé des rétines de rat pour évaluer les réseaux de photodiodes in vitro, et comment les diodes ont produit des réponses électriques qui sont des indicateurs largement acceptés de l’activité visuelle. Les scientifiques testent actuellement le système sur des rats vivants, en prenant des mesures physiologiques et comportementales, et espèrent trouver un sponsor pour soutenir les tests chez l’homme. Œil bionique — mythes et réalité
Œil bionique — mythes et réalité Pouvez-vous imaginer ce que ressent une personne qui ne voit pas ou ne voit presque pas le monde qui l’entoure ? Cette condition s’appelle la cécité – l’incapacité de percevoir les stimuli visuels due à des troubles pathologiques de l’œil lui-même, des nerfs optiques ou du cerveau. En 1972, l’Organisation mondiale de la santé (OMS) a adopté la définition suivante : une personne est considérée comme aveugle si l’acuité de la vision centrale dans des conditions de correction maximale ne dépasse pas 3/60. Avec cette vision, une personne dans des conditions de lumière du jour avec une correction optique maximale est incapable de compter les doigts à une distance de 3 mètres.
Pouvez-vous imaginer ce que ressent une personne qui ne voit pas ou ne voit presque pas le monde qui l’entoure ? Cette condition s’appelle la cécité – l’incapacité de percevoir les stimuli visuels due à des troubles pathologiques de l’œil lui-même, des nerfs optiques ou du cerveau. En 1972, l’Organisation mondiale de la santé (OMS) a adopté la définition suivante : une personne est considérée comme aveugle si l’acuité de la vision centrale dans des conditions de correction maximale ne dépasse pas 3/60. Avec cette vision, une personne dans des conditions de lumière du jour avec une correction optique maximale est incapable de compter les doigts à une distance de 3 mètres.
Ainsi, pour de tels cas, l’idée d’une stimulation électrique de la rétine ou du cortex visuel a été proposée, la création d’une prothèse qui, par le mécanisme d’action, simule les processus réels de transmission des signaux électriques. Il existe plusieurs variantes d’implants électroniques, chaque année de nouvelles idées apparaissent, mais le terme et l’œil bionique lui-même ont été développés par Daniel Palanker, un membre du personnel de l’Université de Stanford et son groupe de recherche sur la physique biomédicale et les technologies ophtalmiques. L’implantation du modèle d’œil bionique Argus II (soit dit en passant, le seul modèle qui a une marque européenne, mais non certifié en Russie) a été réalisée en Russie en juillet 2017 pour un patient. Et de toutes les sources de diffusion télévisée que nous avons entendues, une personne pourra désormais voir le monde comme avant. Des centaines de personnes sont invitées à mettre un œil bionique, et certaines demandent également à «implanter» les puces pour la super-vision. Alors qu’avons-nous aujourd’hui et le rêve de voir le monde devenir réalité après qu’il a perdu la vue peut-il se réaliser ?
Il existe plusieurs variantes d’implants électroniques, chaque année de nouvelles idées apparaissent, mais le terme et l’œil bionique lui-même ont été développés par Daniel Palanker, un membre du personnel de l’Université de Stanford et son groupe de recherche sur la physique biomédicale et les technologies ophtalmiques. L’implantation du modèle d’œil bionique Argus II (soit dit en passant, le seul modèle qui a une marque européenne, mais non certifié en Russie) a été réalisée en Russie en juillet 2017 pour un patient. Et de toutes les sources de diffusion télévisée que nous avons entendues, une personne pourra désormais voir le monde comme avant. Des centaines de personnes sont invitées à mettre un œil bionique, et certaines demandent également à «implanter» les puces pour la super-vision. Alors qu’avons-nous aujourd’hui et le rêve de voir le monde devenir réalité après qu’il a perdu la vue peut-il se réaliser ?
ASPECTS BIOLOGIQUES DE LA PROTÉSISATION AU DÉTAIL Les bioniques sont appelés prothèses et éléments implantables de parties du corps humain dont l’apparence et la fonction sont similaires à celles d’organes ou de membres réels. Aujourd’hui, les bras, les jambes, le cœur et les organes auditifs bioniques aident avec succès les gens à mener une vie bien remplie. Le but de la création d’un œil électronique est d’aider les malvoyants ayant des problèmes de rétine ou de nerf optique. Implantable à la place de la rétine endommagée, l’appareil devrait remplacer des millions de cellules photoréceptrices de l’œil, si ce n’est à 100 %.
Les bioniques sont appelés prothèses et éléments implantables de parties du corps humain dont l’apparence et la fonction sont similaires à celles d’organes ou de membres réels. Aujourd’hui, les bras, les jambes, le cœur et les organes auditifs bioniques aident avec succès les gens à mener une vie bien remplie. Le but de la création d’un œil électronique est d’aider les malvoyants ayant des problèmes de rétine ou de nerf optique. Implantable à la place de la rétine endommagée, l’appareil devrait remplacer des millions de cellules photoréceptrices de l’œil, si ce n’est à 100 %. La technologie pour les yeux est similaire à celle utilisée dans les aides auditives qui aident les personnes sourdes à entendre. Grâce à elle, les patients sont moins susceptibles de perdre leur vision résiduelle, et ceux qui perdent la vue voient la lumière et ont au moins une certaine capacité à s’orienter dans l’espace.
La technologie pour les yeux est similaire à celle utilisée dans les aides auditives qui aident les personnes sourdes à entendre. Grâce à elle, les patients sont moins susceptibles de perdre leur vision résiduelle, et ceux qui perdent la vue voient la lumière et ont au moins une certaine capacité à s’orienter dans l’espace.
ASPECTS TECHNOLOGIQUES Le principe général de l’œil électronique est le suivant: une caméra miniature est intégrée dans des lunettes spéciales, des informations sur l’image sont transmises à l’appareil, qui convertit l’image en un signal électronique et l’envoie à un émetteur spécial, qui à son tour envoie un signal électronique à un œil implanté ou au cerveau du récepteur, ou des informations sont transmises par de minuscules fils aux électrodes attachées à la rétine, ils stimulent les nerfs restants de la rétine en envoyant des impulsions électriques aux nerfs optiques coupés du cerveau. L’appareil est conçu pour compenser les sensations visuelles perdues avec une perte de vision complète ou incomplète.
Le principe général de l’œil électronique est le suivant: une caméra miniature est intégrée dans des lunettes spéciales, des informations sur l’image sont transmises à l’appareil, qui convertit l’image en un signal électronique et l’envoie à un émetteur spécial, qui à son tour envoie un signal électronique à un œil implanté ou au cerveau du récepteur, ou des informations sont transmises par de minuscules fils aux électrodes attachées à la rétine, ils stimulent les nerfs restants de la rétine en envoyant des impulsions électriques aux nerfs optiques coupés du cerveau. L’appareil est conçu pour compenser les sensations visuelles perdues avec une perte de vision complète ou incomplète. Les principales conditions de bon fonctionnement du système:
Les principales conditions de bon fonctionnement du système:
- The presence in the patient’s eye and brain of a part of living nerve cells.
- Patients should be people who once were normally seen, since those who are blind from birth cannot use such devices. Suitable people who have long seen and have a rich visual experience. As a result, they see little, but they have an idea about objects and guess what kind of object it is. In short, the cerebral cortex and the possession of sufficient intelligence must be developed.
- And, of course, the more pixels there will be in the chip, the clearer the resulting image will be.

- Long service life — while nobody knows the life of these devices. The first implantation of bionic eyes in Germany ended with the fact that after a year all patients were removed. Even to those who saw something. This was even written in the German press.
- Technological method of charging. Now they work on the principle of induction, not on batteries. Charged like an electric toothbrush.
- Along the way, the issue of oxidation, heating, etc. should be addressed. For example, a perforated structure after implantation may allow the retinal nerve cells to automatically flow from the upper and lower surfaces of the photosensor through the cavities and connect, as well as reduce the heating of the pixels and increase their number.
ASPECTS MICROCHIRURGICAUX DE LA PROTHÈSE Ce sont les opérations les plus étendues. Si vous décrivez, par exemple, l’implantation d’un œil bionique sous-rétinien (situé sous la rétine) – vous devez soulever complètement la rétine, puis effectuer une rétinectomie étendue (couper une partie de la rétine), puis installer cette puce sous la rétine , puis rétinez la rétine avec un laser rétinien, collez la rétine avec coagulation au laser et versez de l’huile de silicone. Un tamponnement au silicone est nécessaire, sinon la PVR (vitréorétinopathie proliférante) apparaîtra instantanément et un détachement se produira. Oui, il ne devrait pas non plus y avoir de lentille propre, ou elle devrait être pré-remplacée par une lentille artificielle. Pour l’opération, vous avez besoin d’outils spéciaux avec des pointes en silicone douces.
Ce sont les opérations les plus étendues. Si vous décrivez, par exemple, l’implantation d’un œil bionique sous-rétinien (situé sous la rétine) – vous devez soulever complètement la rétine, puis effectuer une rétinectomie étendue (couper une partie de la rétine), puis installer cette puce sous la rétine , puis rétinez la rétine avec un laser rétinien, collez la rétine avec coagulation au laser et versez de l’huile de silicone. Un tamponnement au silicone est nécessaire, sinon la PVR (vitréorétinopathie proliférante) apparaîtra instantanément et un détachement se produira. Oui, il ne devrait pas non plus y avoir de lentille propre, ou elle devrait être pré-remplacée par une lentille artificielle. Pour l’opération, vous avez besoin d’outils spéciaux avec des pointes en silicone douces. 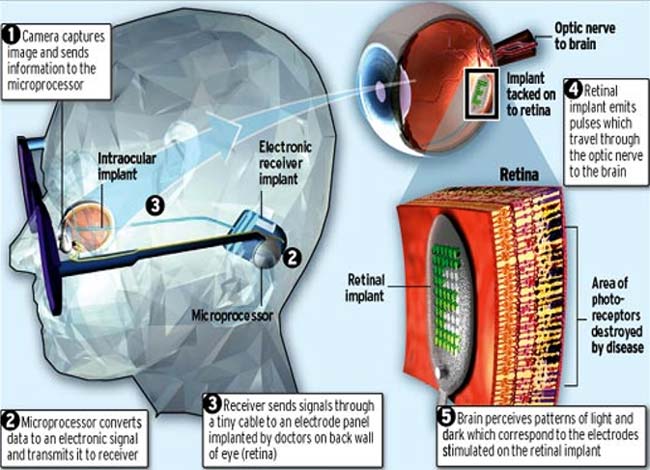 C’est une opération complètement difficile, de plus, un chirurgien orofacial ou un ORL est également nécessaire – ils font sortir les électrodes à travers la peau. Et il s’avère qu’un tel appareil – la puce à l’intérieur de l’œil, et entre les mains d’un tel appareil de la taille d’un téléphone portable, avec lequel vous pouvez modifier l’intensité du signal, se connecte aux électrodes sous-cutanées. Un ophtalmologiste-chirurgien pendant l’opération ne suffit pas – l’aide d’autres disciplines est nécessaire, l’opération dure 6 heures.
C’est une opération complètement difficile, de plus, un chirurgien orofacial ou un ORL est également nécessaire – ils font sortir les électrodes à travers la peau. Et il s’avère qu’un tel appareil – la puce à l’intérieur de l’œil, et entre les mains d’un tel appareil de la taille d’un téléphone portable, avec lequel vous pouvez modifier l’intensité du signal, se connecte aux électrodes sous-cutanées. Un ophtalmologiste-chirurgien pendant l’opération ne suffit pas – l’aide d’autres disciplines est nécessaire, l’opération dure 6 heures.
ASPECTS ÉCONOMIQUES DE LA PROTHÈSE
- Tout d’abord, c’est cher. Seul l’appareil coûte environ 150 000 dollars, soit près de 8,5 millions de roubles. Et tout le traitement d’un tel patient peut atteindre 10 millions de roubles. Il s’agit d’un modèle Argus II. Aujourd’hui, dans certains pays, par exemple en Allemagne, cette opération est prise en charge par une assurance.
- Les entreprises engagées dans le développement et la production dans le monde entier vivent des subventions de l’État, des subventions. C’est formidable – de telles choses devraient être soutenues, sinon il n’y aura pas de développement.
- Il n’y a pas de certificat en Russie pour aucun des appareils suivants.
ASPECTS MÉDICAUX DE LA PROTHÈSE
1. Les résultats sont assez modestes – après l’opération, ces personnes ne peuvent pas être qualifiées de voyantes, elles voient un maximum de 0,05, c’est-à-dire qu’elles peuvent voir les contours et déterminer la direction du mouvement de l’ombre, ne distinguent pas du tout les couleurs, les objets peuvent ne diffèrent que ceux dont on se souvient de l’ancienne vie «voyante», par exemple: «aha – c’est probablement une banane, car quelque chose est semi-circulaire». Ils voient que quelque chose bouge sur eux, ils peuvent deviner qu’il s’agit d’un homme, mais son visage ne se distingue pas.
2. Dans quelles maladies un œil bionique peut-il être utile ? Les premiers patients sont des patients atteints de rétinite pigmentaire (retinitis pigmentoza), une maladie avec une disparition primaire des photorécepteurs et une atrophie secondaire du nerf optique. En Russie, il y a 20 à 30 000 patients de ce type, en Allemagne, il n’y en a que quelques milliers. Viennent ensuite les patients atteints de dégénérescence maculaire atrophique géographique. Il s’agit d’une pathologie de l’âge extrêmement courante de l’œil. Le troisième sera des patients atteints de glaucome. Le glaucome n’a pas encore été étudié, car l’atrophie du nerf optique dans ce cas est primaire, le mode de transmission doit donc être différent – en contournant le nerf optique.  Le diabète est le problème le plus difficile à résoudre. L’une des méthodes de traitement des changements diabétiques sur la rétine est la coagulation au laser sur toute la surface. Après une telle procédure, il est techniquement impossible de soulever la rétine à cause des coagulants – cela se traduit par un «tamis». Et si ce n’est pas fait par un laser, la situation n’est pas meilleure : généralement l’œil est tellement endommagé que l’implantation est inutile dans ce cas.
Le diabète est le problème le plus difficile à résoudre. L’une des méthodes de traitement des changements diabétiques sur la rétine est la coagulation au laser sur toute la surface. Après une telle procédure, il est techniquement impossible de soulever la rétine à cause des coagulants – cela se traduit par un «tamis». Et si ce n’est pas fait par un laser, la situation n’est pas meilleure : généralement l’œil est tellement endommagé que l’implantation est inutile dans ce cas.
3. Malheureusement, le prototype actuel de l’œil bionique ne permet pas aux gens de voir le monde qui nous entoure tel que nous le voyons. Leur objectif est de se déplacer de façon autonome sans aide. Jusqu’à ce que l’utilisation massive de cette technologie soit loin, cependant, les scientifiques donneront de l’espoir aux personnes qui ont perdu la vue.
PROJETS EN COURS DE «BIONIC EYES» Au cours des dernières décennies, des scientifiques de différents pays ont travaillé sur les idées des yeux électroniques bioniques. Chaque fois, les technologies sont améliorées, mais personne n’a encore introduit son produit sur le marché pour une utilisation de masse.
Au cours des dernières décennies, des scientifiques de différents pays ont travaillé sur les idées des yeux électroniques bioniques. Chaque fois, les technologies sont améliorées, mais personne n’a encore introduit son produit sur le marché pour une utilisation de masse.
1. Prothèse rétinienne Argus La prothèse rétinienne Argus est un projet américain assez bien commercialisé. Le premier modèle a été développé par une équipe de chercheurs au début des années 1990 : l’ophtalmologiste d’origine pakistanaise Mark Hameiun (Mark Humayun, soit dit en passant, le professeur Sekundo le connaît à l’Université Johns Hopkins — à l’époque, il était résident du 2e année, Walter était étudiant) Eugen Dayan, l’ingénieur Howard Phillips, le bio-ingénieur Ventay Lew et Robert Greenberg. Le premier modèle, sorti à la fin des années 1990, par Second Sight n’avait que 16 électrodes. Les «essais sur le terrain» de la première version de la rétine bionique ont été menés par Mark Hameiun sur six patients atteints de perte de vision à la suite d’une rétinite pigmentaire entre 2002 et 2004. La rétinite pigmentaire est une maladie incurable dans laquelle une personne perd la vue. Il est observé dans environ un cas pour trois mille cinq cents personnes.
L’apparence du poste extérieur Argus II.
Les patients qui ont été implantés avec un œil bionique ont montré la capacité non seulement de faire la distinction entre la lumière et le mouvement, mais aussi de déterminer des objets de la taille d’une tasse de thé ou même d’un couteau.
Le dispositif de test a été amélioré – au lieu des seize électrodes photosensibles, soixante électrodes y ont été montées et appelées Argus II. En 2007, une étude multicentrique a été lancée dans 10 centres de 4 pays aux États-Unis et en Europe – un total de 30 patients. En 2012, Argus II a reçu l’autorisation d’utilisation commerciale en Europe, un an plus tard en 2013 — aux États-Unis. En Russie, il n’y a pas d’autorisation.
À ce jour, ces études sont subventionnées par des fonds gouvernementaux. Aux États-Unis, il y en a trois – le National Eye Institute, le Department of Energy et la National Science Foundation, ainsi qu’un certain nombre de laboratoires de recherche. Il ressemble à une puce à la surface de la rétine
Il ressemble à une puce à la surface de la rétine
2. Prothèse visuelle basée sur un microsystème (MIVP)
Le modèle de prothèse a été conçu par Claude Veraart à l’Université de Louvain comme un brassard en spirale d’électrodes autour du nerf optique à l’arrière de l’œil. Il se connecte à un stimulateur implanté dans un petit trou du crâne. Le stimulateur reçoit des signaux d’une caméra externe, qui sont traduits en signaux électriques qui stimulent directement le nerf optique.
3. Télescope miniature implantable En fait, ce dispositif ne peut pas être qualifié de « prothèse rétinienne », puisque ce télescope est implanté dans la chambre arrière de l’œil et fonctionne comme une loupe qui augmente l’image rétinienne de 2,2 ou 2,7 fois, ce qui permet de réduire la effet sur la vision des bovins (taches aveugles) dans la partie centrale. Implanté dans un seul œil, car la présence d’un télescope nuit à la vision périphérique. Le deuxième œil travaille pour la périphérie. Implanté par une assez grande incision de la cornée.
En fait, ce dispositif ne peut pas être qualifié de « prothèse rétinienne », puisque ce télescope est implanté dans la chambre arrière de l’œil et fonctionne comme une loupe qui augmente l’image rétinienne de 2,2 ou 2,7 fois, ce qui permet de réduire la effet sur la vision des bovins (taches aveugles) dans la partie centrale. Implanté dans un seul œil, car la présence d’un télescope nuit à la vision périphérique. Le deuxième œil travaille pour la périphérie. Implanté par une assez grande incision de la cornée.
Soit dit en passant, un principe similaire est utilisé dans les lentilles intraoculaires Shariott supplémentaires. J’ai la plus vaste expérience de l’implantation de ces lentilles en Russie et les patients sont satisfaits des résultats. Dans ce cas, une phacoémulsification de la cataracte est d’abord réalisée. Bien qu’il ne s’agisse bien sûr pas d’un œil 100% bionique.
Vision bionique Des équipes de recherche du monde entier développent des substituts électroniques pour la vue. Voici quelques-unes des avancées les plus prometteuses.
Des équipes de recherche du monde entier développent des substituts électroniques pour la vue. Voici quelques-unes des avancées les plus prometteuses.
La recherche sur l’œil bionique a atteint un point de basculement : après des décennies d’exploration et de développement minutieux, 2 prothèses visuelles rétiniennes sont sur le marché en Europe et aux États-Unis et, début 2016, plus de 20 équipes à travers le monde étaient activement engagées dans ce champ d’enquête.  Leurs efforts sont suffisamment robustes – et le nombre de personnes atteintes de déficience visuelle dans le monde est, à 285 millions, 1suffisamment important – pour que le marché mondial des implants rétiniens devrait atteindre plus d’un milliard de dollars d’ici 2022. Et même si les chercheurs sont attention de noter que la vision apportée par ces appareils est, du moins à l’heure actuelle, relativement rudimentaire, ils sont encouragés par le rythme de développement et les applications potentielles.
Leurs efforts sont suffisamment robustes – et le nombre de personnes atteintes de déficience visuelle dans le monde est, à 285 millions, 1suffisamment important – pour que le marché mondial des implants rétiniens devrait atteindre plus d’un milliard de dollars d’ici 2022. Et même si les chercheurs sont attention de noter que la vision apportée par ces appareils est, du moins à l’heure actuelle, relativement rudimentaire, ils sont encouragés par le rythme de développement et les applications potentielles.
Stratégies chirurgicales
Plusieurs équipes au travail signifient que plusieurs stratégies – et plusieurs emplacements chirurgicaux pour l’implantation et la stimulation – sont poursuivies. La plupart des dispositifs ciblent la rétine et peuvent généralement être caractérisés comme épirétiniens, sous-rétiniens ou suprachoroïdiens, selon l’emplacement de leurs composants internes. Cependant, une autre approche innovante contourne complètement la rétine et implique une stimulation directe du cortex visuel.
Placement épirétinien
Les prothèses épirétiniennes sont placées sur la face antérieure de la rétine, où elles stimulent les cellules ganglionnaires. Coup de projecteur sur la recherche : Argus II. Il s’agit peut-être de la prothèse rétinienne la plus connue, car elle a été la première à être approuvée pour une utilisation aux États-Unis et en Europe. Le dispositif, développé par Second Sight, se compose d’un équipement électronique externe porté par l’utilisateur et d’éléments internes implantés dans et sur l’œil. 3 Les éléments externes comprennent une caméra vidéo qui est montée sur une paire de lunettes ; les éléments internes sont un réseau de 6 × 10 mm de 60 électrodes qui est fixé sur la macula et un boîtier électronique et une bobine d’implant attachés à une bande sclérale suturée sur la paroi de l’œil. En raison de sa conception, le destinataire doit utiliser le balayage de la tête pour acquérir des informations visuelles.
Coup de projecteur sur la recherche : Argus II. Il s’agit peut-être de la prothèse rétinienne la plus connue, car elle a été la première à être approuvée pour une utilisation aux États-Unis et en Europe. Le dispositif, développé par Second Sight, se compose d’un équipement électronique externe porté par l’utilisateur et d’éléments internes implantés dans et sur l’œil. 3 Les éléments externes comprennent une caméra vidéo qui est montée sur une paire de lunettes ; les éléments internes sont un réseau de 6 × 10 mm de 60 électrodes qui est fixé sur la macula et un boîtier électronique et une bobine d’implant attachés à une bande sclérale suturée sur la paroi de l’œil. En raison de sa conception, le destinataire doit utiliser le balayage de la tête pour acquérir des informations visuelles.
Applications visées. L’Argus II est approuvé uniquement pour les patients atteints d’une maladie dégénérative de la rétine externe telle que la rétinite pigmentaire (RP) et la choroïdérémie. Les chercheurs étudient actuellement son utilisation dans la dégénérescence maculaire liée à l’âge (DMLA) sèche.
Considérations chirurgicales. Les critères d’inclusion sont « assez spécifiques », a déclaré K. Thiran Jayasundera, MD, de l’Université du Michigan. « Vous devez avoir une perception de la lumière nue et vous ne pouvez pas avoir de problèmes de nerf optique. » De plus, les mesures de longueur axiale d’un patient doivent se situer dans certains paramètres, et la preuve d’une fonction rétinienne de la couche interne intacte doit être confirmée avant l’implantation.
Alors que les événements indésirables ont inclus l’hypotonie, la déhiscence conjonctivale, l’érosion conjonctivale et l’endophtalmie présumée, 3 « les événements indésirables sont assez faibles, en fait, avec une bonne technique chirurgicale », a déclaré le Dr Jayasundera, qui a implanté le dispositif. Il a noté que le placement correct du boîtier électronique et de la bobine réceptrice est «essentiel au placement du réseau à l’intérieur; le tableau tombe sur la macula si ces éléments sont en bonne position sur la sclérotique. Il a ajouté que « la fermeture de la sclérotomie est très importante, car il peut y avoir une fuite à travers une sclérotomie ouverte ».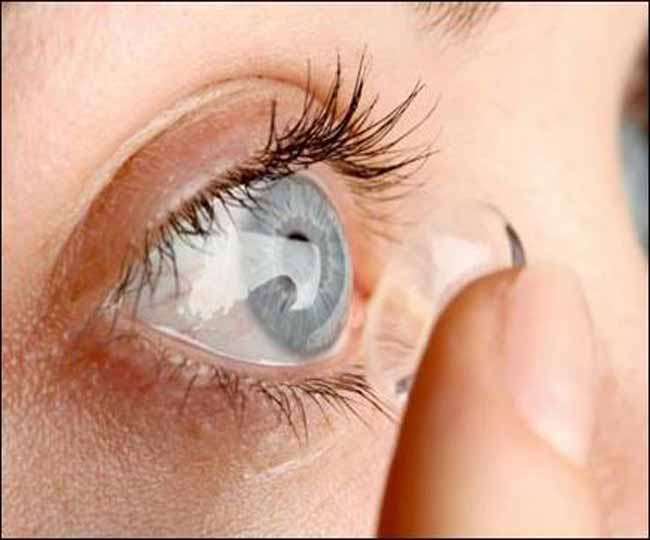 Statut actuel. L’Argus II a été implanté chez plus de 190 patients dans le monde. Les résultats à ce jour indiquent que le dispositif reste une option raisonnablement fiable et stable pour les patients atteints de PR avancée. Dans un récent suivi de 5 ans de 30 patients ayant reçu l’Argus, 3 celui-ci est resté en place et fonctionnel chez 24. Deux dispositifs ont échoué et 3 ont été explantés en raison d’événements indésirables (1 patient est décédé de causes non liées). Dans les tests de mobilité fonctionnels « suivez la porte » et « suivez la ligne », les patients ont pu manœuvrer avec plus de succès lorsque le système était allumé que lorsqu’il était éteint.
Statut actuel. L’Argus II a été implanté chez plus de 190 patients dans le monde. Les résultats à ce jour indiquent que le dispositif reste une option raisonnablement fiable et stable pour les patients atteints de PR avancée. Dans un récent suivi de 5 ans de 30 patients ayant reçu l’Argus, 3 celui-ci est resté en place et fonctionnel chez 24. Deux dispositifs ont échoué et 3 ont été explantés en raison d’événements indésirables (1 patient est décédé de causes non liées). Dans les tests de mobilité fonctionnels « suivez la porte » et « suivez la ligne », les patients ont pu manœuvrer avec plus de succès lorsque le système était allumé que lorsqu’il était éteint.
En ce qui concerne l’extension de l’utilisation, les premiers résultats d’une étude portant sur 4 patients atteints de DMLA sèche à un stade avancé ont révélé que la fonction de vision centrale était déclenchée par l’appareil sur la zone d’atrophie géographique sous-fovéale. 4 Et les améliorations de l’appareil se poursuivent : Second Sight travaille sur une nouvelle itération qui inclura des algorithmes mis à jour, a déclaré le Dr Jayasundera.
Appareils similaires en développement. L’implant épirétinien Iris-II (Pixium Vision) est en essai clinique en Europe. L’appareil, qui est également conçu pour les patients atteints de RP, possède 150 électrodes et une conception facilement explantable.
Placement sous-rétinien
Les dispositifs sous-rétiniens sont placés sous l’épithélium pigmentaire rétinien dans la couche photoréceptrice.
Coup de projecteur sur la recherche : Alpha-IMS. Cette prothèse, développée par Retina Implant en Allemagne, possède une micropuce de 3 × 3 mm qui est implantée en position sous-fovéale. La puce contient 1 500 photodiodes photosensibles reliées à des microélectrodes. La prothèse Alpha-IMS n’utilise pas de caméra externe ; au lieu de cela, les photodiodes sont couplées à un module d’alimentation externe qui est implanté sous la peau derrière l’oreille et amplifie les signaux générés par le réseau de photodiodes.
La prothèse Alpha-IMS n’utilise pas de caméra externe ; au lieu de cela, les photodiodes sont couplées à un module d’alimentation externe qui est implanté sous la peau derrière l’oreille et amplifie les signaux générés par le réseau de photodiodes.
L’un des avantages de l’Alpha-IMS est que le patient n’a pas besoin d’utiliser le balayage de la tête pour localiser des objets ; à la place, des mouvements oculaires normaux peuvent être utilisés. « L’image se déplace avec l’œil car la puce est intégrée exactement là où les photorécepteurs se trouveraient normalement », a déclaré Robert E. MacLaren, MD, de l’Université d’Oxford en Angleterre. « En scannant une image avec des saccades, les patients peuvent en tirer plus d’informations que ce ne serait le cas avec une image statique. »
En ce qui concerne la procédure d’implantation, « La chirurgie est complexe, mais tout chirurgien vitréo-rétinien à haut volume devrait pouvoir l’apprendre. L’aide d’un chirurgien implanteur cochléaire est également nécessaire pour placer l’alimentation électrique sous la peau derrière l’oreille », a déclaré le Dr MacLaren, qui participe aux essais cliniques d’une nouvelle version de l’appareil. Pour le chirurgien de la rétine, il a déclaré : « La partie la plus difficile est de positionner la puce sous la rétine, mais c’est important car dans cette position, les signaux électroniques transmis par la puce sont dirigés vers les cellules bipolaires, qui profitent de la rétine naturelle. traitement. » Applications visées. La prothèse Alpha-IMS est approuvée en Europe pour les patients atteints de RP. Une version plus récente, l’Alpha-AMS, est en cours d’essais cliniques. Le Dr MacLaren a indiqué qu’il implantait actuellement la puce AMS, qui est plus grande et contient 1 600 pixels, dans le cadre d’une étude financée par le National Health Service du Royaume-Uni.
Applications visées. La prothèse Alpha-IMS est approuvée en Europe pour les patients atteints de RP. Une version plus récente, l’Alpha-AMS, est en cours d’essais cliniques. Le Dr MacLaren a indiqué qu’il implantait actuellement la puce AMS, qui est plus grande et contient 1 600 pixels, dans le cadre d’une étude financée par le National Health Service du Royaume-Uni.
Statut actuel. En 2015, les chercheurs d’Alpha-IMS ont rapporté des résultats sur 12 mois avec 29 patients. 5 Treize des destinataires étaient capables de reconnaître des formes et des détails d’objets dans la vie quotidienne, et 8 pouvaient localiser des objets à contraste élevé mais ne pouvaient pas reconnaître des formes ou des détails. « J’ai vu plusieurs patients qui n’avaient aucune perception de la lumière revoir soudainement des choses », a déclaré le Dr MacLaren. « Les formes et les contours des objets peuvent sembler une vision rudimentaire pour vous et moi, mais pour quelqu’un qui est complètement aveugle, c’est un moment qui change la vie. » Il a ajouté : « À ce jour, tous les patients ont pu voir des choses avec la puce. De plus, il n’y a eu aucun problème avec l’anesthésie, bien que ce soit une longue opération. Jusqu’à présent, 29 patients ont reçu l’Alpha-IMS et 15 ont reçu l’Alpha-AMS.
Jusqu’à présent, 29 patients ont reçu l’Alpha-IMS et 15 ont reçu l’Alpha-AMS.
 Appareils similaires en développement. Des chercheurs de Stanford ont mis au point une prothèse sous-rétinienne photovoltaïque sans fil. Les bénéficiaires porteront des lunettes qui capturent des images et les projettent dans l’œil et sur un réseau de photodiodes implantées ; la lumière est ensuite convertie en courant pulsé, qui stimule les neurones rétiniens internes. 6 La prothèse, baptisée Prima, est en cours de préparation pour des essais cliniques en collaboration avec Pixium Vision.
Appareils similaires en développement. Des chercheurs de Stanford ont mis au point une prothèse sous-rétinienne photovoltaïque sans fil. Les bénéficiaires porteront des lunettes qui capturent des images et les projettent dans l’œil et sur un réseau de photodiodes implantées ; la lumière est ensuite convertie en courant pulsé, qui stimule les neurones rétiniens internes. 6 La prothèse, baptisée Prima, est en cours de préparation pour des essais cliniques en collaboration avec Pixium Vision.
Il y a eu de nombreux progrès dans le traitement des maladies qui entraînent une déficience visuelle. Ces traitements préviennent ou limitent l’étendue de la déficience visuelle.83,84 Les options, cependant, sont limitées une fois qu’une personne a perdu la vision. La prothèse visuelle est une approche radicale et innovante pour redonner la vision à ces personnes.
Australian scientists implant early prototype of a "bionic eye" into a patient
https://habr.com/en/companies/klinika_shilovoy/articles/511188/
https://www.sciencedaily.com/releases/2012/08/120831065003.htm
https://www.aao.org/eyenet/article/bionic-vision
https://onlinelibrary.wiley.com/doi/full/10.1111/j.1442-9071.2011.02590.x
